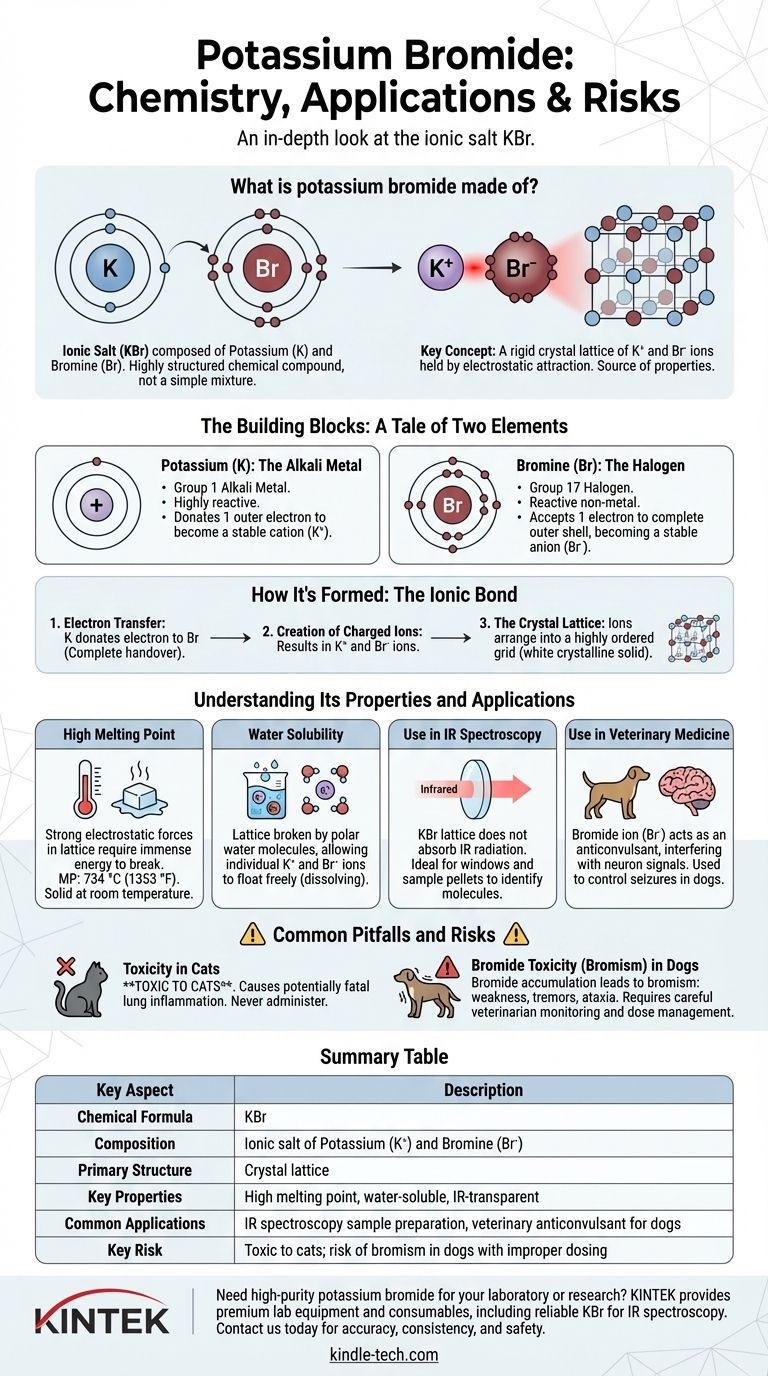
باختصار، بروميد البوتاسيوم هو ملح أيوني يتكون من عنصري البوتاسيوم والبروم. وهو ليس مجرد خليط بسيط بل مركب كيميائي ذو بنية عالية بالصيغة KBr. تمنح ذرة البوتاسيوم إلكترونًا لذرة البروم، مما يخلق جسيمات مشحونة (أيونات) يتم تثبيتها معًا بواسطة تجاذب إلكتروستاتيكي قوي.
يكمن مفتاح فهم بروميد البوتاسيوم في رؤيته ليس كمجموعة من الذرات، بل كشبكة بلورية صلبة من أيونات البوتاسيوم الموجبة الشحنة وأيونات البروميد السالبة الشحنة. هذا التركيب الأيوني هو مصدر أهم خصائصه وتطبيقاته.

اللبنات الأساسية: حكاية عنصرين
وجود بروميد البوتاسيوم هو نتيجة مباشرة للخصائص الكيميائية الأساسية للعنصرين المكونين له. لكل منهما "رغبة" قوية في تحقيق تكوين إلكتروني أكثر استقرارًا.
البوتاسيوم (K): الفلز القلوي
البوتاسيوم هو فلز ناعم وشديد التفاعل يوجد في المجموعة 1 من الجدول الدوري. خاصيته المميزة هي امتلاكه إلكترونًا واحدًا في غلافه الخارجي.
يكون أكثر استقرارًا من الناحية الطاقية إذا تخلص من هذا الإلكترون الوحيد. وبقيامه بذلك، يصبح أيونًا موجب الشحنة (K⁺).
البروم (Br): الهالوجين
البروم هو لا فلز تفاعلي من المجموعة 17، وهي مجموعة الهالوجينات. ميزته المميزة هي امتلاكه سبعة إلكترونات في غلافه الخارجي، أي أقل بإلكترون واحد فقط من مجموعة كاملة ومستقرة من ثمانية إلكترونات.
يقبل بسهولة إلكترونًا لإكمال هذا الغلاف، ليصبح أيونًا سالب الشحنة (Br⁻)، يُعرف باسم أيون البروميد.
كيف يتكون: الرابطة الأيونية
تكوين بروميد البوتاسيوم هو مثال كلاسيكي للرابطة الأيونية، والتي تُعرَّف بنقل الإلكترونات وليس بمشاركتها.
نقل الإلكترون
عندما يتفاعل فلز البوتاسيوم والبروم، تتبرع كل ذرة بوتاسيوم بإلكترونها الخارجي الوحيد لذرة بروم. هذا ليس مشاركة لطيفة بل تسليمًا كاملاً.
إنشاء الأيونات المشحونة
يؤدي نقل الإلكترون هذا إلى تكوين جسيمين مستقرين، ولكنهما مشحونان الآن: كاتيون البوتاسيوم (K⁺) وأنيون البروميد (Br⁻). ونظرًا لتجاذب الشحنات المتعاكسة، فإنهما ينجذبان بقوة لبعضهما البعض.
الشبكة البلورية
هذه الأيونات الموجبة والسالبة لا تشكل أزواجًا بسيطة. بدلاً من ذلك، ترتب نفسها في شبكة ثلاثية الأبعاد منظمة للغاية ومتكررة تسمى الشبكة البلورية. هذا الهيكل القوي والصلب هو ما يجعل بروميد البوتاسيوم مادة صلبة بلورية بيضاء في درجة حرارة الغرفة.
فهم خصائصه وتطبيقاته
الطبيعة الأيونية لبروميد البوتاسيوم تفسر مباشرة سلوكه الفيزيائي والكيميائي، والذي بدوره يحدد استخداماته.
نقطة انصهار عالية
القوى الكهروستاتيكية القوية التي تربط أيونات K⁺ و Br⁻ معًا في الشبكة البلورية تتطلب كمية هائلة من الطاقة لكسرها. ولهذا السبب، فإن KBr مادة صلبة ذات نقطة انصهار عالية تبلغ 734 درجة مئوية (1353 درجة فهرنهايت).
الذوبان في الماء
على الرغم من أن الشبكة قوية، إلا أنه يمكن تفكيكها بواسطة الجزيئات القطبية مثل الماء. تحيط جزيئات الماء بأيونات K⁺ و Br⁻ الفردية، وتحيّد شحنتها وتسمح لها بالتحرك بحرية، وهو ما ندركه على أنه ذوبان الملح.
الاستخدام في مطيافية الأشعة تحت الحمراء
لا تمتص الشبكة البلورية لـ KBr إشعاع الأشعة تحت الحمراء. هذا الشفافية تجعله مادة مثالية لإنشاء النوافذ وبلورات العينات المستخدمة في مطيافية الأشعة تحت الحمراء، وهي تقنية تساعد الكيميائيين على تحديد الجزيئات.
الاستخدام في الطب البيطري
يمكن لأيون البروميد (Br⁻) أن يعمل كمضاد للتشنج عن طريق التدخل في نقل أيونات الكلوريد في الخلايا العصبية للجهاز العصبي المركزي. لهذا السبب، يستخدم KBr في الطب البيطري للسيطرة على النوبات لدى الكلاب.
المزالق والمخاطر الشائعة
على الرغم من فائدته، فإن بروميد البوتاسيوم ليس خاليًا من المخاطر، ومن الضروري فهمها في تطبيقاته العملية.
السمية لدى القطط
الخطر الأساسي يكمن في الاستخدام البيطري. بروميد البوتاسيوم سام للقطط، مسببًا حالة التهاب رئوي قد تكون قاتلة. يجب عدم إعطاؤه لها أبدًا.
تسمم البروميد (البرومية) لدى الكلاب
حتى في الكلاب، حيث يستخدم علاجيًا، يمكن أن يتراكم أيون البروميد في الجسم بمرور الوقت. إذا أصبحت المستويات مرتفعة للغاية، فقد يؤدي ذلك إلى حالة تسمى البرومية، مع أعراض مثل الضعف والرعشة والرنح. يتطلب هذا إدارة دقيقة للجرعة ومراقبة من قبل طبيب بيطري.
كيفية تطبيق هذه المعرفة
سيعتمد منظورك لبروميد البوتاسيوم كليًا على هدفك.
- إذا كان تركيزك الأساسي هو الكيمياء: انظر إليه كمثال نموذجي للرابطة الأيونية المتكونة بين فلز قلوي من المجموعة 1 وهالوجين من المجموعة 17.
- إذا كان تركيزك الأساسي هو التحليل المخبري: أدرك أن شفافيته للأشعة تحت الحمراء وقدرته على الضغط في قرص صلب هي الخصائص الرئيسية التي تجعله لا يقدر بثمن لإعداد العينات.
- إذا كان تركيزك الأساسي هو الصحة البيطرية: افهم أن تأثيره العلاجي يأتي من أيون البروميد، ولكن هذا لا ينفصل عن الخطر الجسيم للسمية، خاصة في القطط.
في نهاية المطاف، معرفة أن KBr مبني من أيونات منقولة بين فلز ولا فلز هي الأساس لفهم كل استخدام له وحدوده.
جدول ملخص:
| الجانب الرئيسي | الوصف |
|---|---|
| الصيغة الكيميائية | KBr |
| التكوين | ملح أيوني من البوتاسيوم (K⁺) والبروم (Br⁻) |
| الهيكل الأساسي | شبكة بلورية |
| الخصائص الرئيسية | نقطة انصهار عالية، قابل للذوبان في الماء، شفاف للأشعة تحت الحمراء |
| التطبيقات الشائعة | إعداد عينات مطيافية الأشعة تحت الحمراء، مضاد للتشنج البيطري للكلاب |
| الخطر الرئيسي | سام للقطط؛ خطر البرومية لدى الكلاب مع الجرعات غير الصحيحة |
هل تحتاج إلى بروميد بوتاسيوم عالي النقاء لمختبرك أو أبحاثك؟ تتخصص KINTEK في توفير معدات ومواد استهلاكية مخبرية متميزة، بما في ذلك KBr الموثوق به لمطيافية الأشعة تحت الحمراء والتطبيقات الأخرى. تضمن منتجاتنا الدقة والاتساق والسلامة لعملك. اتصل بنا اليوم لمعرفة كيف يمكننا دعم احتياجات مختبرك بالمواد والخبرة المناسبة.
دليل مرئي
المنتجات ذات الصلة
- قطب مرجعي كالوميل كلوريد الفضة كبريتات الزئبق للاستخدام المخبري
- مواد الماس المطعمة بالبورون بتقنية الترسيب الكيميائي للبخار (CVD)
- حمام مائي متعدد الوظائف للخلية الكهروكيميائية بطبقة واحدة أو مزدوجة
- قطب مرجعي لكبريتات النحاس للاستخدام المخبري
- مكبس هيدروليكي أوتوماتيكي للمختبرات لضغط حبيبات XRF و KBR
يسأل الناس أيضًا
- أي قطب يستخدم كقطب مرجعي؟ دليل للقياسات الكهروكيميائية الدقيقة
- ما هي الصيانة الموصى بها لمحلول التعبئة الخاص بقطب مرجعي؟ دليل للحصول على قراءات مستقرة ودقيقة
- ما هو الغرض من القطب المرجعي؟ تحقيق قياسات كهروكيميائية مستقرة ودقيقة
- كيف يرتبط اختيار الأقطاب المرجعية، مثل Ag/AgCl أو Hg/HgO، بدرجة حموضة الإلكتروليت في اختبار تفاعل تطور الهيدروجين (HER)؟
- أي قطب يستخدم كمرجع أرضي؟ أتقن مفتاح القياسات الكهروكيميائية الدقيقة



















