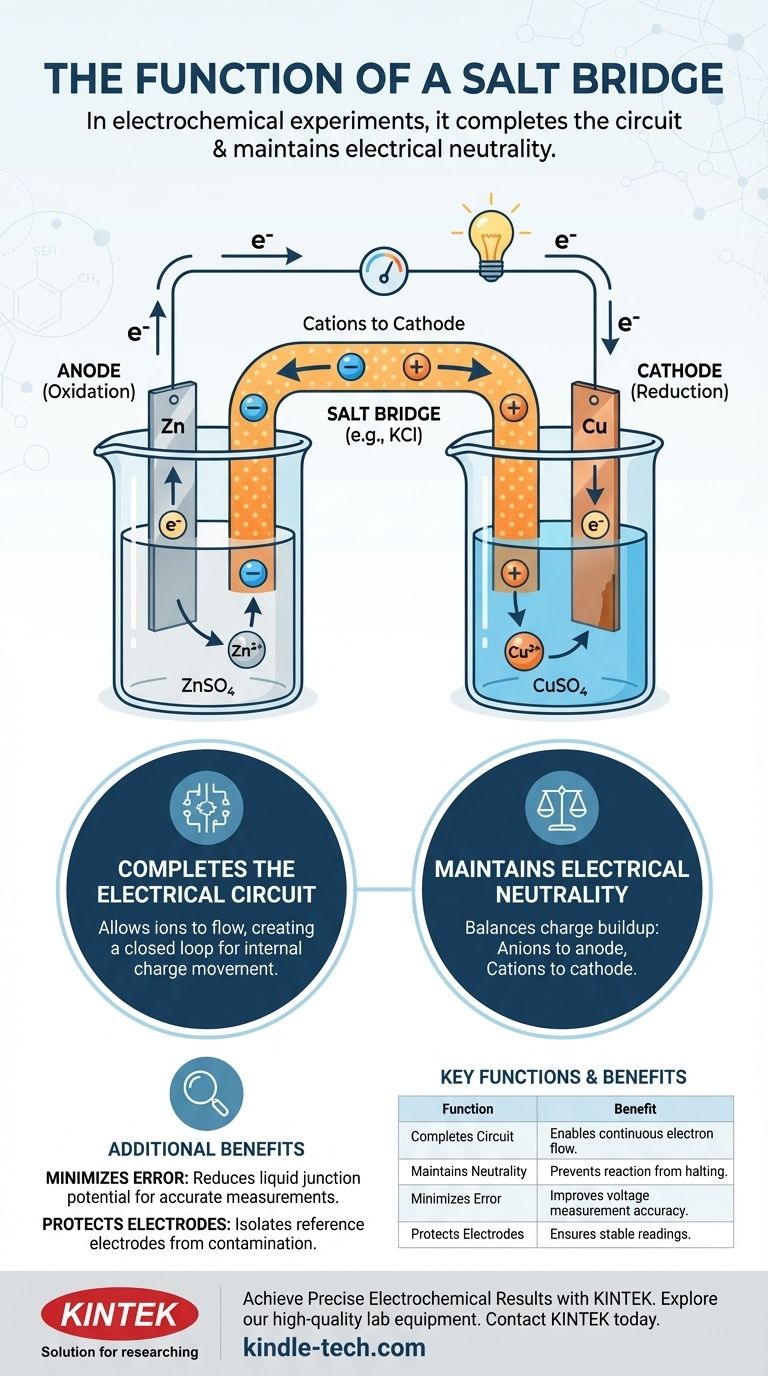
في التجارب الكهروكيميائية، يخدم الجسر الملحي وظيفتين أساسيتين: إكمال الدائرة الكهربائية عن طريق السماح للأيونات بالتدفق بين نصفي الخلية، والحفاظ على الحياد الكهربائي في كل نصف خلية. بدون هذا المكون الحاسم، ستتراكم الشحنة بسرعة، مما يوقف تدفق الإلكترونات ويوقف التفاعل الكهروكيميائي على الفور تقريبًا.
الجسر الملحي ليس مجرد موصل؛ بل هو آلية موازنة الشحنة التي تجعل التفاعل الكهروكيميائي المستدام ممكنًا. إنه يعمل داخليًا، وينقل الأيونات لمواجهة اختلال التوازن في الشحنة الناجم عن حركة الإلكترونات خارجيًا.

تشريح الخلية الكهروكيميائية
لفهم وظيفة الجسر الملحي، يجب عليك أولاً تصور النظام الذي يعمل فيه. الخلية الكهروكيميائية هي في الأساس جهاز يحول الطاقة الكيميائية إلى طاقة كهربائية، أو العكس.
نصفا الخلية
تتكون الخلية الكهروكيميائية من نصفي خلية. يحتوي كل نصف خلية عادةً على قطب كهربائي (موصل صلب مثل الزنك أو النحاس) مغمور في محلول إلكتروليتي (محلول يحتوي على أيونات، مثل كبريتات الزنك أو كبريتات النحاس).
في نصف خلية واحدة، يحدث الأكسدة (فقدان الإلكترونات)، ويسمى هذا القطب الأنود. وفي النصف الآخر، تحدث الاختزال (اكتساب الإلكترونات)، وهذا القطب هو الكاثود.
المشكلة: تراكم الشحنة الفوري
تنتقل الإلكترونات المتولدة عند الأنود عبر سلك خارجي إلى الكاثود، مما يخلق تيارًا كهربائيًا. ومع ذلك، يخلق تدفق الإلكترون هذا مشكلة فورية.
مع فقدان الأنود للإلكترونات، يتراكم محلول الإلكتروليت الخاص به بزيادة من الأيونات الموجبة. وعلى العكس من ذلك، مع اكتساب الكاثود للإلكترونات، يطور محلول الإلكتروليت الخاص به فائضًا من الأيونات السالبة (حيث يتم استهلاك الأيونات الموجبة من المحلول). يخلق هذا الفصل للشحنة جهدًا معاكسًا قويًا يوقف تدفق الإلكترونات تمامًا.
الوظائف الأساسية للجسر الملحي
الجسر الملحي هو الحل الأنيق لمشكلة تراكم الشحنة هذه. وهو عادةً أنبوب على شكل حرف U مملوء بمحلول مركز من إلكتروليت خامل، مثل كلوريد البوتاسيوم (KCl) أو نترات البوتاسيوم (KNO₃).
إكمال الدائرة الكهربائية
تتطلب الدائرة الكهربائية المكتملة حلقة مغلقة. يسمح السلك الخارجي للإلكترونات بالتدفق، لكن هذا ليس سوى نصف الدائرة. يكمل الجسر الملحي الحلقة عن طريق السماح للأيونات بالتدفق بين نصفي الخلية، مما يخلق مسارًا لحركة الشحنة داخليًا.
الحفاظ على الحياد الكهربائي
هذه هي الوظيفة الأكثر أهمية للجسر الملحي. لمعادلة الشحنة المتراكمة:
- الأنيونات (الأيونات السالبة) من الجسر الملحي تهاجر إلى نصف خلية الأنود لموازنة الأيونات الموجبة الزائدة التي تتكون.
- الكاتيونات (الأيونات الموجبة) من الجسر الملحي تهاجر إلى نصف خلية الكاثود لموازنة الشحنة السالبة الزائدة.
من خلال موازنة الشحنة باستمرار في نصفي الخلية، يضمن الجسر الملحي إمكانية استمرار التفاعل الكهروكيميائي والحفاظ على تيار ثابت.
تقليل جهد الوصلة السائلة
في القياسات الأكثر دقة، يعمل الجسر الملحي أيضًا على تقليل جهد الوصلة السائلة. هذا جهد صغير وغير مرغوب فيه يتشكل عند واجهة محلولين إلكتروليتيين مختلفين. من خلال إنشاء جسر أيوني أكثر تدرجًا، فإنه يقلل من مصدر الخطأ هذا، مما يؤدي إلى قياسات جهد أكثر دقة للخلية.
فهم الاعتبارات العملية
تعتمد فعالية الجسر الملحي كليًا على تكوينه وتفاعله مع بقية الخلية.
يجب أن يكون الإلكتروليت خاملًا
يجب ألا تتفاعل الأيونات الموجودة داخل الجسر الملحي مع الأيونات الموجودة في أي من محاليل نصفي الخلية. على سبيل المثال، استخدام جسر ملحي KCl في خلية تحتوي على نترات الفضة (AgNO₃) سيكون خطأ. ستتفاعل أيونات الكلوريد (Cl⁻) مع أيونات الفضة (Ag⁺) لتكوين راسب صلب (AgCl)، مما يعطل وظيفة الخلية.
حماية القطب المرجعي
في الإعداد ثلاثي الأقطاب الشائع في الكيمياء الكهربائية، غالبًا ما يستخدم الجسر الملحي لتوصيل قطب مرجعي (الذي له جهد ثابت ومعروف) بالمحلول الرئيسي. يتم ذلك لعزل القطب المرجعي، ومنع الأيونات من محلول الاختبار من تلويثه وتغيير جهده المستقر. هذا يطيل عمر القطب الكهربائي ويضمن دقة القياس.
اتخاذ الخيار الصحيح لتجربتك
الدور الأساسي للجسر الملحي هو دائمًا تسهيل تدفق الأيونات، ولكن يمكن النظر إلى أهميته من خلال عدسات مختلفة اعتمادًا على هدفك.
- إذا كان تركيزك الأساسي هو عرض خلية جلفانية بسيطة: فكر في الجسر الملحي على أنه المكون الذي يكمل الدائرة ويسمح للبطارية بالعمل باستمرار.
- إذا كان تركيزك الأساسي هو قياس الجهد الدقيق: فإن الجسر الملحي ضروري لتقليل جهد الوصلة السائلة، وهو مصدر رئيسي لخطأ التجربة.
- إذا كان تركيزك الأساسي هو الكيمياء الكهربائية التحليلية (مثل دراسات التآكل): فإن الجسر الملحي ضروري لعزل قطبك المرجعي لضمان حصولك على خط أساس مستقر وموثوق لقراءات الجهد الخاصة بك.
في نهاية المطاف، يتيح الجسر الملحي الدراسة المنضبطة والمستمرة للتفاعلات الكهروكيميائية عن طريق حل المشكلة الأساسية المتمثلة في فصل الشحنة.
جدول الملخص:
| الوظيفة | الوصف | الفائدة الرئيسية |
|---|---|---|
| إكمال الدائرة | يسمح بتدفق الأيونات بين نصفي الخلية. | يمكّن تدفق الإلكترونات المستمر. |
| الحفاظ على الحياد | يوازن تراكم الشحنة الناتج عن نقل الإلكترون. | يمنع توقف التفاعل. |
| تقليل الخطأ | يقلل من جهد الوصلة السائلة. | يحسن دقة قياس الجهد. |
| حماية الأقطاب | يعزل الأقطاب المرجعية عن التلوث. | يضمن قراءات مستقرة وموثوقة. |
هل أنت مستعد لتحقيق نتائج دقيقة وموثوقة في تجاربك الكهروكيميائية؟ المعدات المناسبة أساسية لنجاحك. تتخصص KINTEK في المعدات والمواد الاستهلاكية المخبرية عالية الجودة، بما في ذلك الخلايا الكهروكيميائية والملحقات المصممة للدقة والمتانة. دع خبرائنا يساعدونك في اختيار الإعداد المثالي لاحتياجاتك البحثية.
اتصل بـ KINTEK اليوم لمناقشة كيف يمكننا دعم القدرات الكهروكيميائية لمختبرك!
دليل مرئي