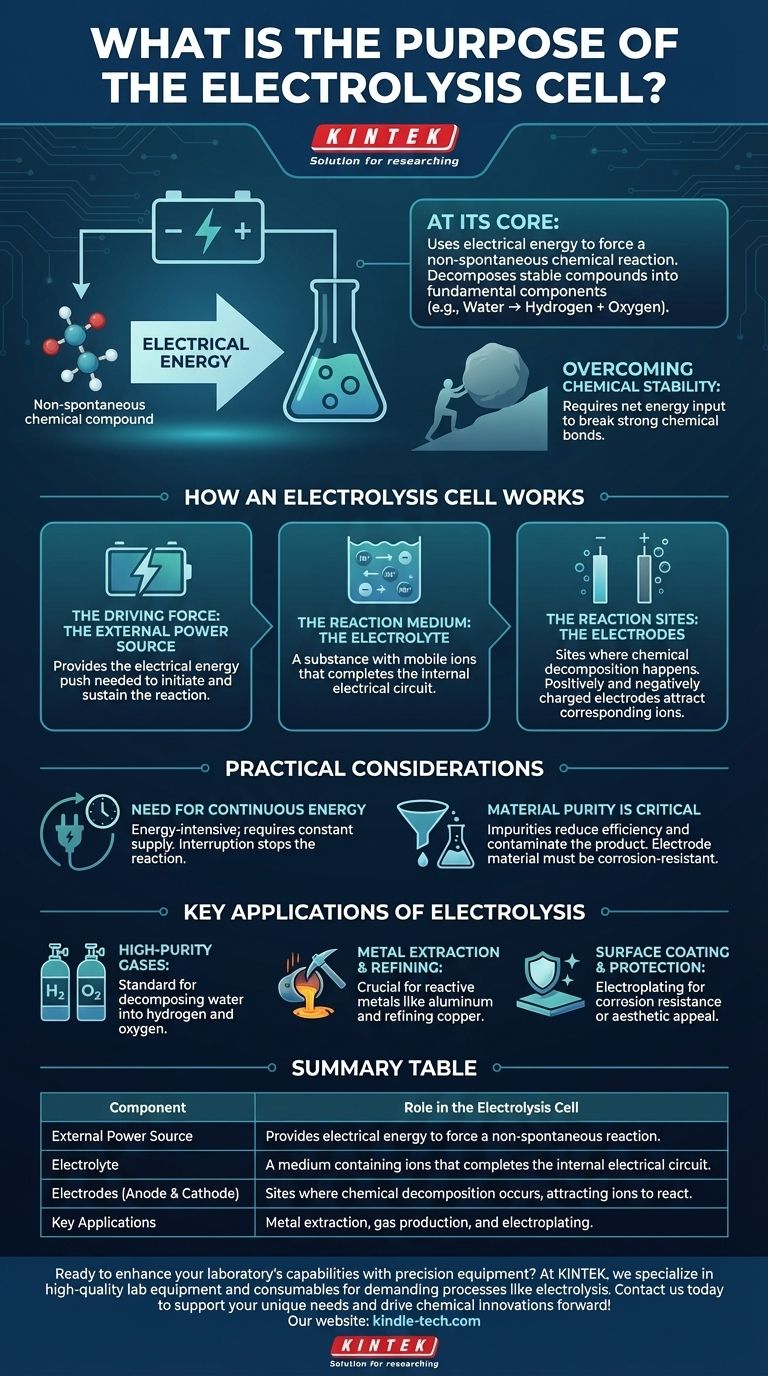
في جوهرها، الغرض من خلية التحليل الكهربائي هو استخدام الطاقة الكهربائية لإجبار تفاعل كيميائي لن يحدث من تلقاء نفسه. هذه العملية، المعروفة باسم التحليل الكهربائي، تسمح لنا بتحليل المركبات الكيميائية المستقرة إلى مكوناتها الأساسية، مثل تحليل الماء إلى هيدروجين وأكسجين.
بينما تطلق العديد من التفاعلات الكيميائية الطاقة، تتطلب بعض أهم العمليات الصناعية إدخال طاقة للمضي قدمًا. خلية التحليل الكهربائي هي الأداة الأساسية المصممة لتوفير هذه الطاقة، باستخدام الكهرباء لدفع التفاعلات غير التلقائية وإنشاء منتجات كيميائية قيمة.

كيف تعمل خلية التحليل الكهربائي
خلية التحليل الكهربائي هي نظام يتكون من ثلاثة مكونات حاسمة تعمل معًا لتحقيق تغيير كيميائي محدد. فهم كل جزء يوضح العملية برمتها.
القوة الدافعة: مصدر الطاقة الخارجي
يوفر مصدر طاقة خارجي، مثل بطارية، الطاقة الكهربائية المطلوبة. تعمل هذه الطاقة كـ "دفعة" ضرورية لبدء واستدامة تفاعل كيميائي غير مواتٍ للطاقة. بدون هذا الجهد الخارجي، لن يحدث التحلل.
وسط التفاعل: الإلكتروليت
الإلكتروليت هو الوسط الذي يتيح تدفق الجسيمات المشحونة (الأيونات). إنه ليس مجرد سائل؛ إنه مادة، عادة ما تكون محلولًا من الأملاح المذابة في الماء أو ملحًا مصهورًا، يحتوي على أيونات متحركة. هذه الحركة للأيونات بين الأقطاب هي ما يكمل الدائرة الكهربائية داخل الخلية.
مواقع التفاعل: الأقطاب الكهربائية
يتم غمر قطبين كهربائيين (مصعد ومهبط) في الإلكتروليت. هذه هي المواقع المادية التي يحدث فيها التحلل الكيميائي بالفعل. عند تطبيق مصدر الطاقة الخارجي، يصبح أحد الأقطاب موجب الشحنة والآخر سالب الشحنة، مما يجذب الأيونات المقابلة من الإلكتروليت ويجبرها على التفاعل.
الهدف الأساسي: إجبار تفاعل غير تلقائي
الغرض الكامل من الخلية هو التغلب على الاستقرار الطبيعي للمركب. هذا هو الفرق الرئيسي بين الخلية الإلكتروليتية والخلية الجلفانية (مثل البطارية القياسية)، التي تطلق الطاقة من تفاعل تلقائي.
التغلب على الاستقرار الكيميائي
التفاعل غير التلقائي هو تفاعل يتطلب إدخالًا صافيًا للطاقة للمضي قدمًا. فكر في الأمر كدفع صخرة صعودًا - لن يحدث من تلقاء نفسه. توفر الطاقة الكهربائية الموردة لخلية التحليل الكهربائي القوة اللازمة لدفع هذه "الصخرة الكيميائية" صعودًا، وكسر الروابط الكيميائية القوية.
معنى التحليل الكهربائي
الاسم نفسه يفسر الوظيفة. يأتي من "إلكترو"، في إشارة إلى الكهرباء، والكلمة اليونانية "lysis"، التي تعني التفكك أو التحلل. تستخدم الخلية الكهرباء لتفكيك مركب.
فهم الاعتبارات العملية
على الرغم من قوتها، فإن التحليل الكهربائي لا يخلو من متطلباته وقيوده. تطبيقها هو خيار هندسي متعمد يعتمد على مقايضات محددة.
الحاجة إلى طاقة مستمرة
التحليل الكهربائي عملية كثيفة الاستهلاك للطاقة. تتطلب إمدادًا ثابتًا وغالبًا ما يكون كبيرًا من الكهرباء للتشغيل. إذا انقطع التيار الكهربائي، يتوقف التفاعل على الفور. تكلفة الطاقة هذه هي عامل أساسي في الجدوى الاقتصادية للتحليل الكهربائي الصناعي.
نقاء المواد أمر بالغ الأهمية
نقاء الإلكتروليت أمر بالغ الأهمية. يمكن أن تؤدي الشوائب إلى تفاعلات جانبية غير مرغوب فيها، مما يقلل من كفاءة العملية الرئيسية ويلوث المنتج النهائي. اختيار مادة القطب الكهربائي أمر حيوي أيضًا، حيث يجب أن يتحمل البيئة المسببة للتآكل وألا يتداخل مع التفاعل المطلوب.
التطبيقات الرئيسية للتحليل الكهربائي
يعتمد التطبيق الصحيح كليًا على هدفك النهائي. تعدد استخدامات التحليل الكهربائي يجعله حجر الزاوية في الكيمياء والصناعة الحديثة.
- إذا كان تركيزك الأساسي هو إنتاج غازات عالية النقاء: التحليل الكهربائي هو الطريقة القياسية لتحليل الماء (H₂O) إلى هيدروجين وأكسجين نقيين للغاية.
- إذا كان تركيزك الأساسي هو استخلاص المعادن وتكريرها: العملية لا غنى عنها لإنتاج معادن عالية التفاعل مثل الألومنيوم من خامها (البوكسيت) أو تكرير النحاس إلى درجة نقاء عالية.
- إذا كان تركيزك الأساسي هو طلاء السطح وحمايته: تستخدم عملية تحليل كهربائي مماثلة، تُعرف بالطلاء الكهربائي، لترسيب طبقة رقيقة من معدن واحد (مثل الكروم أو الذهب) على معدن آخر لمقاومة التآكل أو للجاذبية الجمالية.
في النهاية، خلية التحليل الكهربائي هي أداة أساسية لتحويل الطاقة الكهربائية إلى تغيير كيميائي قيم، مما يمكننا من إنشاء مواد لا تنتجها الطبيعة من تلقاء نفسها.
جدول الملخص:
| المكون | الدور في خلية التحليل الكهربائي |
|---|---|
| مصدر الطاقة الخارجي | يوفر الطاقة الكهربائية لإجبار تفاعل غير تلقائي. |
| الإلكتروليت | وسط يحتوي على أيونات يكمل الدائرة الكهربائية الداخلية. |
| الأقطاب الكهربائية (المصعد والمهبط) | المواقع التي يحدث فيها التحلل الكيميائي، وتجذب الأيونات للتفاعل. |
| التطبيقات الرئيسية | استخلاص المعادن (مثل الألومنيوم)، إنتاج الغاز (مثل الهيدروجين)، والطلاء الكهربائي. |
هل أنت مستعد لتعزيز قدرات مختبرك بمعدات دقيقة؟ في KINTEK، نحن متخصصون في توفير معدات ومستهلكات مختبرية عالية الجودة مصممة للعمليات الصعبة مثل التحليل الكهربائي. سواء كنت تقوم بتكرير المعادن، أو إنتاج غازات عالية النقاء، أو إجراء الطلاء الكهربائي، فإن أدواتنا الموثوقة تضمن الكفاءة والدقة. اتصل بنا اليوم لاكتشاف كيف يمكن لـ KINTEK دعم الاحتياجات الفريدة لمختبرك ودفع ابتكاراتك الكيميائية إلى الأمام!
دليل مرئي
المنتجات ذات الصلة
- خلايا التحليل الكهربائي PEM قابلة للتخصيص لتطبيقات بحثية متنوعة
- خلية التحليل الكهربائي الطيفي بالطبقة الرقيقة
- خلية غاز الانتشار الكهروكيميائية التحليلية خلية تفاعل سائل
- خلية كهروكيميائية كهروكيميائية كوارتز للتجارب الكهروكيميائية
- خلية التحليل الكهربائي من PTFE خلية كهروكيميائية مقاومة للتآكل مختومة وغير مختومة
يسأل الناس أيضًا
- ما هو إجراء التنظيف الفوري بعد الاستخدام لخلية التحليل الكهربائي؟ منع تراكم البقايا للحصول على نتائج دقيقة
- ما هي خلية التحليل الكهربائي؟ دليل لدفع التفاعلات الكيميائية بالكهرباء
- ما هي تكوينات الفتحات للإصدارات غير المحكمة والغلق المحكم لخلية التحليل الكهربائي؟ حسّن إعدادك الكهروكيميائي
- ما هي مخاطر التحكم غير السليم في الجهد في خلية التحليل الكهربائي؟ تجنب التلف المكلف وعدم الكفاءة
- ماذا يُعرف أيضًا بخلية التحليل الكهربائي؟ فهم الخلايا التحليلية مقابل الخلايا الغلفانية



















