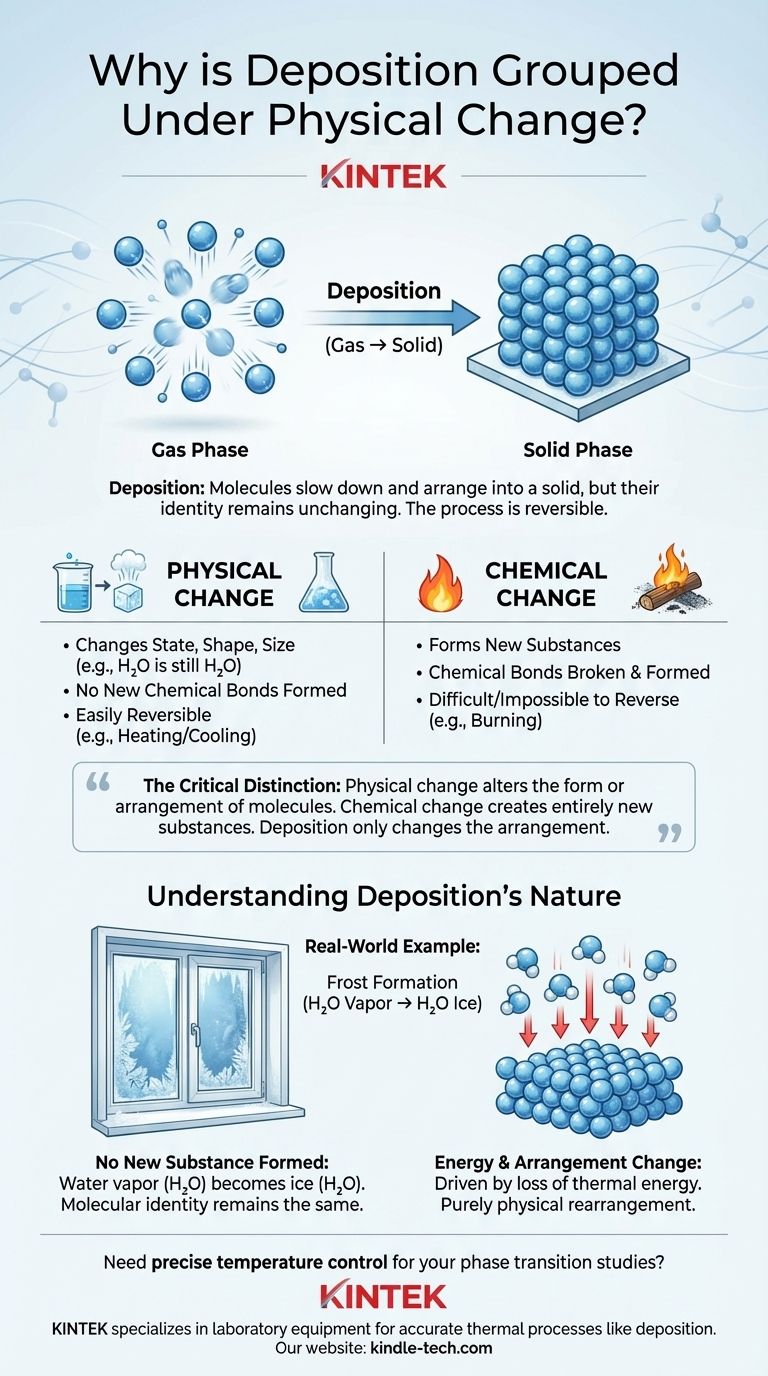
يُصنف الترسيب كتغير فيزيائي لأنه يغير فقط حالة المادة، وليس هويتها الكيميائية الأساسية. أثناء الترسيب، تنتقل جزيئات المادة مباشرة من الحالة الغازية إلى الحالة الصلبة، مما يغير ترتيبها ومستوى طاقتها، لكن الجزيئات نفسها تظل سليمة وغير متغيرة.
التمييز الحاسم هو: التغير الفيزيائي يغير شكل أو ترتيب الجزيئات، بينما التغير الكيميائي يكسر ويشكل روابط لإنشاء مواد جديدة تمامًا. الترسيب يغير الترتيب فقط.

الخط الفاصل: التغير الفيزيائي مقابل التغير الكيميائي
لفهم سبب وقوع الترسيب بشكل مباشر ضمن الفئة الفيزيائية، يجب علينا أولاً وضع تعريف واضح لكلا النوعين من التغيرات. يعود التمييز إلى ما يحدث على المستوى الجزيئي.
ما الذي يشكل التغير الفيزيائي؟
يؤثر التغير الفيزيائي على الخصائص الفيزيائية للمادة دون تغيير تركيبها الكيميائي. ترتبط هذه التغيرات بشكل أساسي بالطاقة وترتيب الجسيمات.
تشمل الخصائص الرئيسية التغيرات في الحالة (صلبة، سائلة، غازية)، الشكل، أو الحجم. مثال كلاسيكي هو الماء: الجليد، الماء السائل، وبخار الماء كلها H₂O. فقط تباعد وطاقة الجزيئات هي التي تغيرت.
غالبًا ما تكون هذه التغيرات قابلة للعكس بسهولة بوسائل فيزيائية، مثل التسخين أو التبريد.
ما الذي يشكل التغير الكيميائي؟
ينتج عن التغير الكيميائي، أو التفاعل الكيميائي، تكوين مادة أو أكثر جديدة تمامًا بخصائص وتركيبات مختلفة.
تتضمن هذه العملية كسر الروابط الكيميائية الموجودة وتكوين روابط جديدة. على سبيل المثال، عندما يحترق الخشب، فإنه يتفاعل مع الأكسجين ليصبح رمادًا وثاني أكسيد الكربون وماء - مواد تختلف كيميائيًا عن الخشب الأصلي.
عادة ما يكون من الصعب أو المستحيل عكس التغيرات الكيميائية بوسائل فيزيائية بسيطة.
تحليل الترسيب على المستوى الجزيئي
عندما نطبق هذا الإطار على الترسيب، يصبح تصنيفه واضحًا.
شرح عملية الترسيب
الترسيب هو الانتقال المباشر للمادة من الحالة الغازية إلى الحالة الصلبة، متجاوزًا تمامًا المرحلة السائلة الوسيطة.
مثال شائع في العالم الحقيقي هو تكون الصقيع. في صباح بارد، يتلامس بخار الماء في الهواء (غاز) مع سطح أقل من نقطة التجمد، مثل زجاج النافذة، ويتحول مباشرة إلى بلورات ثلج (صلب).
لا تتكون مواد جديدة
هذه هي النقطة الأكثر أهمية. بخار الماء في الهواء له الصيغة الكيميائية H₂O. بلورات الجليد التي تتكون كصقيع لها أيضًا الصيغة الكيميائية H₂O.
لم تتغير الهوية الجزيئية للمادة. لم يتم كسر أي روابط كيميائية داخل جزيئات الماء، ولم يتم إنشاء مواد جديدة.
إنه تغير في الطاقة والترتيب
يحدث الانتقال بسبب فقدان الطاقة الحرارية. تفقد جزيئات الماء عالية الطاقة وسريعة الحركة في الحالة الغازية الطاقة عند ملامستها للسطح البارد.
يؤدي فقدان الطاقة هذا إلى تباطؤها وترتيب نفسها في بنية بلورية ثابتة ومنظمة - الحالة الصلبة. التغير هو مجرد تغير في الترتيب الفيزيائي والطاقة، وليس التركيب الكيميائي.
فهم المقايضات والمفاهيم الخاطئة الشائعة
يعد الخلط بين التغيرات الفيزيائية والكيميائية أمرًا شائعًا، خاصة عندما يحدث تغير بصري كبير.
مغالطة "المظهر الجديد"
قد تبدو المادة التي تخضع للترسيب، مثل بخار الماء غير المرئي الذي يشكل صقيعًا مرئيًا، وكأن مادة جديدة قد تكونت. ومع ذلك، فإن التغير في المظهر هو سمة مميزة للتغير الفيزيائي.
ركز دائمًا على التركيب الكيميائي، وليس الشكل البصري. اللون والملمس والحالة هي خصائص فيزيائية يمكن أن تتغير دون حدوث أي تفاعل كيميائي.
القابلية للعكس كمؤشر قوي
الترسيب عملية قابلة للعكس. العملية العكسية، حيث يتحول الصلب مباشرة إلى غاز، تسمى التسامي. على سبيل المثال، يتسامى الثلج الجاف (ثاني أكسيد الكربون الصلب) إلى غاز ثاني أكسيد الكربون.
القدرة على عكس العملية ببساطة عن طريق إضافة الطاقة (التسخين) دون تفاعل كيميائي هي دليل قوي على أنك تتعامل مع تغير فيزيائي.
كيفية تصنيف أي تغيير بشكل صحيح
لتحديد ما إذا كانت العملية فيزيائية أم كيميائية، اسأل نفسك سلسلة من الأسئلة المحددة.
- إذا كان تركيزك الأساسي هو تحديد التغير الفيزيائي: اسأل، "هل الصيغة الكيميائية الأساسية للمادة هي نفسها قبل وبعد التغيير؟"
- إذا كان تركيزك الأساسي هو تحديد التغير الكيميائي: اسأل، "هل تم كسر أو تكوين روابط كيميائية لإنشاء مادة جديدة بخصائص مختلفة؟"
- عند الشك في عملية ما: اسأل، "هل يمكن عكس هذا التغيير بسهولة بوسائل فيزيائية بسيطة، مثل التسخين أو التبريد أو الذوبان؟"
التركيز على الهوية غير المتغيرة للجزيئات هو المفتاح للتمييز بدقة بين العمليات الفيزيائية والكيميائية.
جدول الملخص:
| الجانب | التغير الفيزيائي | التغير الكيميائي |
|---|---|---|
| الهوية الجزيئية | تبقى كما هي (مثلاً، H₂O تبقى H₂O) | تتغير (تتكون مواد جديدة) |
| تغيير الروابط | لا يوجد كسر/تكوين للروابط الكيميائية | تُكسر الروابط وتُكوّن روابط جديدة |
| القابلية للعكس | قابلة للعكس بسهولة (مثلاً، التسخين/التبريد) | صعبة أو مستحيلة العكس |
| مثال على العملية | الترسيب (غاز → صلب)، التجمد | الاحتراق، الصدأ، الهضم |
هل تحتاج إلى تحكم دقيق في درجة الحرارة لدراسات انتقال الطور الخاصة بك؟ تتخصص KINTEK في معدات المختبرات والمواد الاستهلاكية المصممة لعمليات حرارية دقيقة مثل الترسيب والتسامي. سواء كنت تبحث في علوم المواد أو تجري تجارب تعليمية، تضمن أدواتنا الموثوقة نتائج متسقة. اتصل بخبرائنا اليوم للعثور على الحل الأمثل لاحتياجات مختبرك!
دليل مرئي