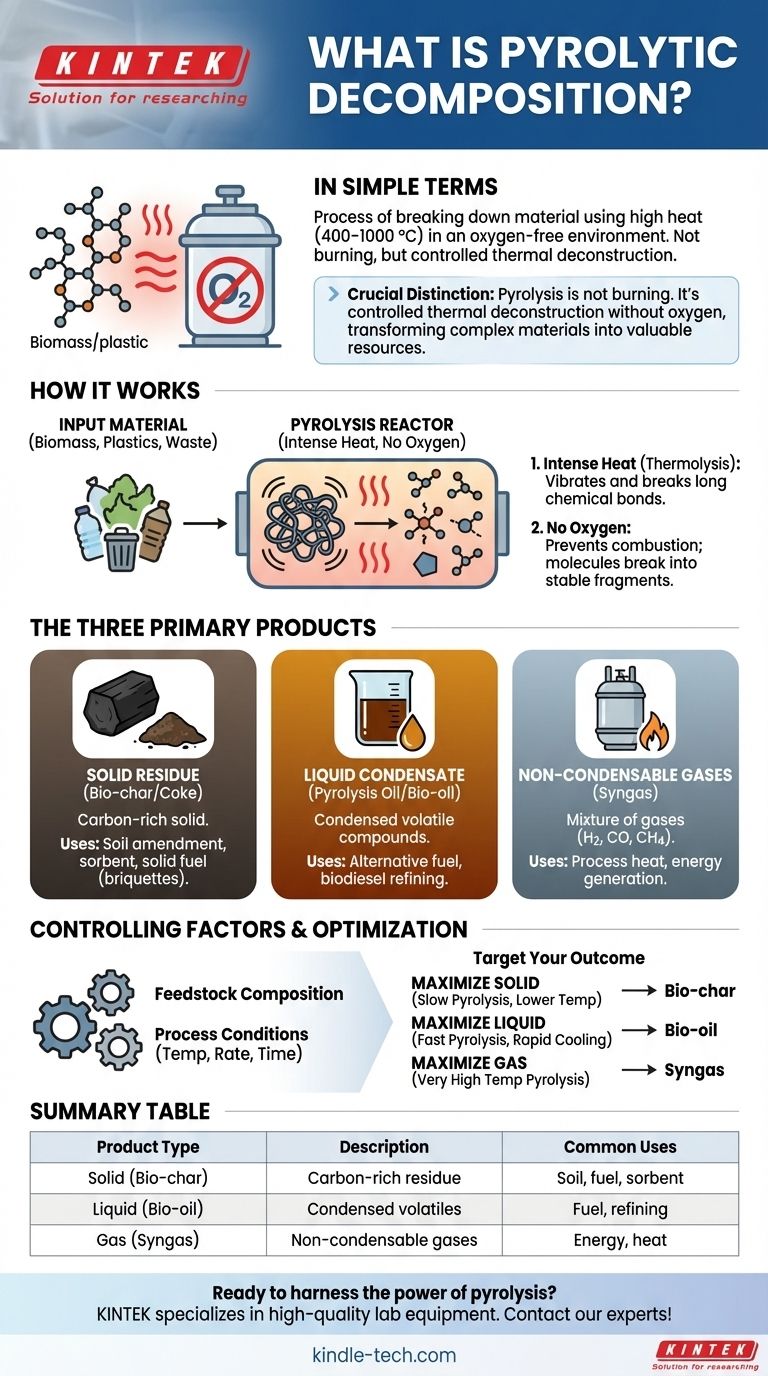
ببساطة، التحلل الحراري الانحلالي، أو الانحلال الحراري، هو عملية تفكيك مادة باستخدام حرارة عالية في بيئة خالية من الأكسجين. بدلاً من الاحتراق، تتكسر الروابط الكيميائية للمادة بفعل الطاقة الحرارية الشديدة (عادةً 400-1000 درجة مئوية)، مما يؤدي إلى تحللها إلى مكونات أبسط وأكثر استقرارًا. تُستخدم هذه التقنية بشكل شائع على المواد المعقدة ذات الوزن الجزيئي العالي مثل الكتلة الحيوية أو البلاستيك أو النفايات.
التمييز الحاسم الذي يجب فهمه هو أن الانحلال الحراري ليس احتراقًا؛ إنه تفكيك حراري مُتحكم به. بمنع الاحتراق في بيئة خالية من الأكسجين، يمكنك تحويل المواد المعقدة إلى مجموعة يمكن التنبؤ بها من المنتجات الصلبة والسائلة والغازية القيمة.

كيف يعمل التحلل الحراري الانحلالي
الانحلال الحراري هو عملية كيميائية حرارية قوية مدفوعة بشرطين أساسيين: الحرارة الشديدة وغياب عامل مؤكسد مثل الأكسجين.
دور الحرارة العالية
الآلية الأساسية للانحلال الحراري هي تطبيق درجات حرارة عالية. هذه الطاقة الحرارية قوية بما يكفي لاهتزاز وتكسير الروابط الكيميائية الطويلة والمعقدة داخل المادة الأصلية، وهي عملية تُعرف باسم التحلل الحراري.
الغياب الحاسم للأكسجين
هذا ما يميز الانحلال الحراري عن الاحتراق. بدون الأكسجين، لا يمكن للمادة أن "تحترق" بالمعنى التقليدي. بدلاً من التفاعل مع الأكسجين لإنتاج النار والرماد والدخان، تتفكك الجزيئات ببساطة إلى أجزاء أصغر وأكثر استقرارًا.
تفكيك الجزيئات المعقدة
هذه الطريقة فعالة بشكل خاص للمواد العضوية أو البوليمرات ذات الأوزان الجزيئية العالية جدًا. يتم تفكيك هذه الجزيئات الكبيرة والضخمة إلى خليط من الجزيئات الأبسط والأصغر، والتي يمكن بعد ذلك جمعها كمنتجات مميزة.
المنتجات الأساسية الثلاثة للانحلال الحراري
ناتج الانحلال الحراري ليس مادة واحدة ولكنه خليط من المواد الصلبة والسائلة والغازات. تعتمد النسب الدقيقة بشكل كبير على المادة الخام وظروف العملية المحددة.
البقايا الصلبة (الفحم الحيوي أو فحم الكوك)
هذه هي المادة الصلبة الغنية بالكربون المتبقية بعد طرد المكونات المتطايرة. إنه منتج مستقر له استخدامات في الزراعة (كمُحسِّن للتربة)، وكمادة ماصة صناعية، أو كمصدر وقود صلب (قوالب).
المكثف السائل (زيت الانحلال الحراري أو الزيت الحيوي)
بعد تكون الغازات المتطايرة، يمكن تبريدها وتكثيفها إلى سائل. هذا الزيت الناتج عن الانحلال الحراري هو خليط معقد من المركبات التي يمكن استخدامها كوقود بديل أو تكريرها بشكل أكبر إلى منتجات ذات قيمة أعلى مثل الديزل الحيوي.
الغازات غير القابلة للتكثف (الغاز الاصطناعي)
هذا خليط من الغازات (مثل الهيدروجين وأول أكسيد الكربون والميثان) التي لا تتكثف مرة أخرى إلى سائل عند التبريد. يتمتع هذا "الغاز الاصطناعي" بقيمة وقود وغالبًا ما يتم التقاطه واستخدامه لتوفير الطاقة الحرارية لعملية الانحلال الحراري نفسها، مما يجعلها مستدامة جزئيًا.
فهم العوامل المتحكمة
بينما العملية بسيطة من حيث المبدأ، يمكن أن تكون النتائج متغيرة للغاية. يتطلب التحكم في النتيجة فهمًا دقيقًا للعوامل الرئيسية.
تركيب المواد الخام هو المفتاح
أكبر عامل يحدد الناتج هو المادة الخام المدخلة. سينتج الانحلال الحراري للخشب زيوتًا وغازات وفحمًا مختلفًا تمامًا مقارنة بالانحلال الحراري للنفايات البلاستيكية أو الإطارات.
ظروف العملية تحدد العوائد
كيفية تطبيق الحرارة مهمة للغاية. ستؤدي درجة الحرارة ومعدل التسخين ومقدار الوقت الذي تقضيه المادة عند تلك الدرجة الحرارة إلى تغيير توازن المنتجات النهائية.
على سبيل المثال، يميل الانحلال الحراري البطيء عند درجات حرارة منخفضة إلى زيادة إنتاج الفحم الحيوي الصلب. في المقابل، يُستخدم الانحلال الحراري السريع متبوعًا بالتبريد السريع لزيادة إنتاج الزيت الحيوي السائل.
اتخاذ القرار الصحيح لهدفك
تعدد استخدامات الانحلال الحراري يعني أنه يمكن تكييفه لتحقيق نتائج مختلفة. يعتمد النهج الأمثل كليًا على المنتج النهائي الذي تقدره أكثر.
- إذا كان تركيزك الأساسي هو إنشاء مُحسِّن للتربة أو كربون صلب: استخدم الانحلال الحراري البطيء ودرجات الحرارة المنخفضة لزيادة إنتاج الفحم الحيوي الصلب.
- إذا كان تركيزك الأساسي هو إنتاج الوقود السائل: استخدم الانحلال الحراري السريع مع التبريد السريع لزيادة جمع الزيت الحيوي والحفاظ عليه.
- إذا كان تركيزك الأساسي هو توليد الطاقة أو غاز التخليق: استخدم الانحلال الحراري عالي الحرارة جدًا لزيادة تحويل المادة إلى غاز غير قابل للتكثف.
في النهاية، يعمل التحلل الحراري الانحلالي كأداة قوية ومرنة لتحويل المواد الخام منخفضة القيمة إلى مجموعة من الموارد القيمة.
جدول الملخص:
| نوع المنتج | الوصف | الاستخدامات الشائعة |
|---|---|---|
| صلب (فحم حيوي/فحم الكوك) | بقايا صلبة غنية بالكربون | مُحسِّن للتربة، مادة ماصة، وقود صلب |
| سائل (زيت حيوي) | مركبات متطايرة مكثفة | وقود بديل، تكرير الديزل الحيوي |
| غاز (غاز اصطناعي) | غازات غير قابلة للتكثف (H2، CO، CH4) | حرارة العملية، توليد الطاقة |
هل أنت مستعد لتسخير قوة الانحلال الحراري في مختبرك؟ تتخصص KINTEK في معدات المختبرات عالية الجودة، بما في ذلك مفاعلات وأفران الانحلال الحراري، لمساعدتك على تحويل الكتلة الحيوية والبلاستيك والمواد الأخرى بكفاءة إلى منتجات قيمة مثل الزيت الحيوي والفحم الحيوي. اتصل بخبرائنا اليوم للعثور على حل الانحلال الحراري المثالي لاحتياجاتك البحثية أو المعالجة!
دليل مرئي
المنتجات ذات الصلة
- فرن دوار كهربائي صغير لتقطير الكتلة الحيوية
- فرن دوار كهربائي يعمل بشكل مستمر مصنع تحلل صغير فرن دوار تسخين
- آلة مصنع فرن الانحلال الحراري بالفرن الدوار الكهربائي، فرن التكليس، فرن دوار صغير، فرن دوار
- نظام معدات ترسيب البخار الكيميائي متعدد الاستخدامات ذو الأنبوب الحراري المصنوع حسب الطلب للعملاء
- آلة مفاعل ترسيب البخار الكيميائي بالبلازما الميكروويف MPCVD للمختبر ونمو الماس
يسأل الناس أيضًا
- كيف يتم تسخين الأفران الدوارة؟ شرح طرق التسخين المباشر مقابل التسخين غير المباشر
- ما هو مفاعل الفرن الدوار؟ دليل للمعالجة الحرارية الصناعية
- ما هي التفاعلات المتضمنة في الانحلال الحراري للكتلة الحيوية؟ اكتشف الكيمياء للمنتجات الحيوية المصممة خصيصًا
- ما هي خصائص أنماط الحركة المنزلقة، والانهيار، والدحرجة للطبقة؟ تحسين عملية الدوران الخاصة بك
- ما هي المفاعلات المستخدمة في الانحلال الحراري السريع؟ اختيار النظام المناسب لتحقيق أقصى قدر من إنتاج الزيت الحيوي








