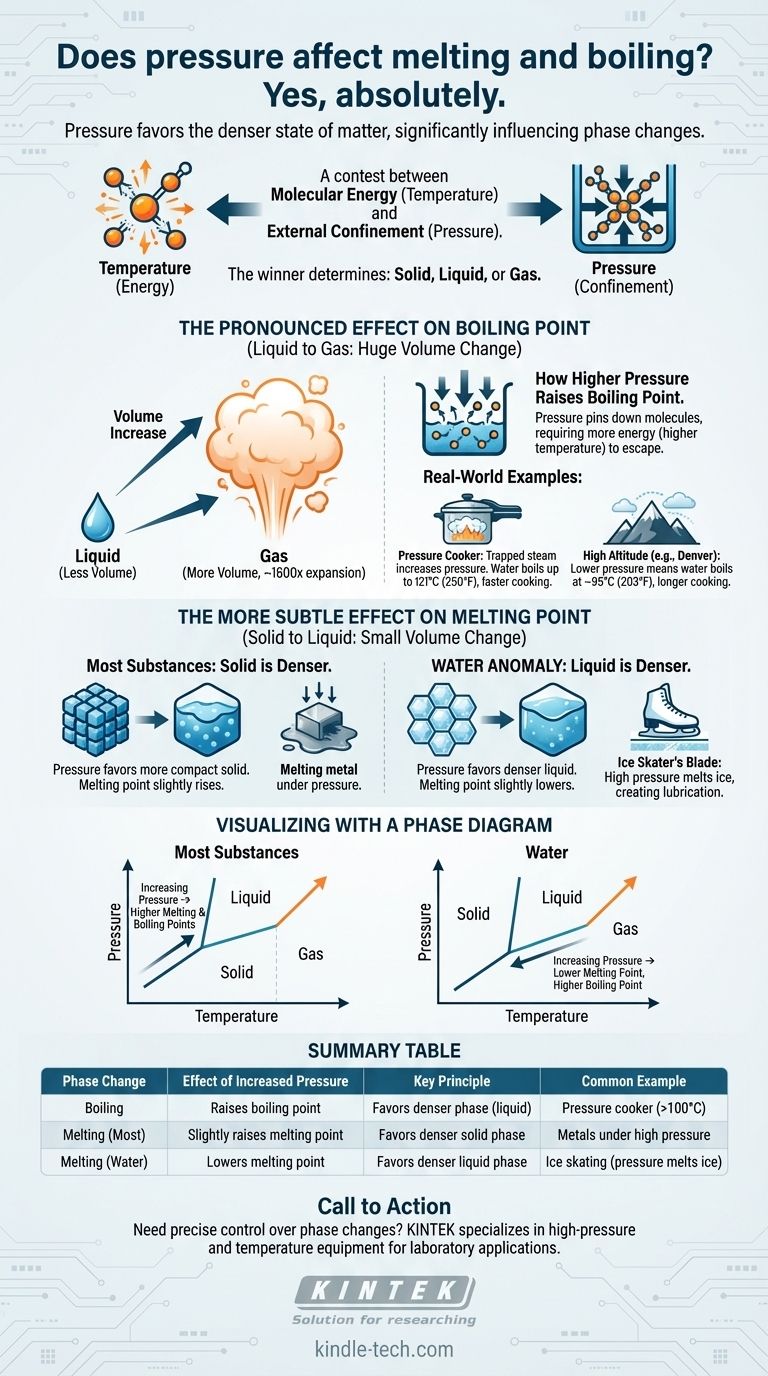
نعم، بالتأكيد. الضغط عامل حاسم يؤثر بشكل مباشر على درجات الحرارة التي تتغير عندها المواد طورها. زيادة الضغط الخارجي ترفع بشكل عام نقطة غليان السائل بشكل كبير. تأثيره على نقطة الانصهار أكثر دقة ولكنه يتبع مبدأً واضحًا: الضغط يفضل الحالة الأكثر كثافة للمادة.
المبدأ الأساسي هو منافسة بين الطاقة الجزيئية (درجة الحرارة) والحبس الخارجي (الضغط). تمنح درجة الحرارة الجزيئات الطاقة اللازمة للتحرر إلى حالة أقل انتظامًا، بينما يجبرها الضغط على التجمع في حالة أكثر تماسكًا وكثافة. يحدد الفائز في هذه المنافسة ما إذا كانت المادة صلبة أو سائلة أو غازية.

لماذا يؤثر الضغط على تغيرات الطور
المعركة بين الطاقة والحبس
يحدث تغير الطور، مثل الانصهار أو الغليان، عندما تكتسب الجزيئات طاقة حرارية كافية للتغلب على القوى التي تربطها في هيكل ثابت. توفر درجة الحرارة هذه الطاقة.
الضغط، من ناحية أخرى، هو قوة خارجية تدفع الجزيئات معًا. إنه يعمل كشكل من أشكال الحبس، مما يجعل من الصعب على الجزيئات الانتشار والتحول إلى طور أقل كثافة.
مسألة الحجم والكثافة
مفتاح فهم تأثير الضغط يكمن في الحجم. عندما تذوب مادة أو تغلي، يتغير حجمها وكثافتها.
سيفضل الضغط دائمًا الطور الذي يشغل حجمًا أقل - الطور الأكثر كثافة. هذه القاعدة الواحدة تفسر سبب تأثير الضغط على الغليان والانصهار بشكل مختلف.
التأثير الواضح على نقطة الغليان
من السائل إلى الغاز: تغير هائل في الحجم
ينطوي الانتقال من سائل إلى غاز على زيادة هائلة في الحجم. قطرة ماء واحدة، على سبيل المثال، تتمدد لتملأ مساحة أكبر بأكثر من 1600 مرة عندما تصبح بخارًا.
نظرًا لأن هذا التغير في الحجم كبير جدًا، فإن للضغط تأثيرًا قويًا ومباشرًا جدًا على نقطة الغليان.
كيف ترفع زيادة الضغط نقطة الغليان
عندما تزيد الضغط على سطح سائل، فإنك في الأساس "تثبت" الجزيئات. تتطلب الآن طاقة حركية أكبر بكثير (درجة حرارة أعلى) للهروب إلى الطور الغازي.
هذا هو السبب في أن نقطة غليان جميع المواد تقريبًا تزداد مع زيادة الضغط.
مثال واقعي: قدر الضغط
يعمل قدر الضغط عن طريق إغلاق وعاء، وحبس البخار الناتج عن غليان الماء. يزيد هذا البخار المحبوس بشكل كبير من الضغط في الداخل.
تحت هذا الضغط العالي، يمكن أن ترتفع نقطة غليان الماء من 100 درجة مئوية (212 درجة فهرنهايت) إلى 121 درجة مئوية (250 درجة فهرنهايت). ينقل هذا الماء الأكثر سخونة الحرارة بسرعة أكبر، مما يقلل بشكل كبير من أوقات الطهي.
مثال واقعي: الطهي على ارتفاعات عالية
يحدث العكس على ارتفاعات عالية. في دنفر، كولورادو (على ارتفاع 5280 قدمًا)، يكون الضغط الجوي أقل.
مع انخفاض الضغط الجوي الذي يثبت جزيئات الماء، يمكنها الهروب إلى الطور الغازي بسهولة أكبر. يغلي الماء هناك عند حوالي 95 درجة مئوية (203 درجة فهرنهايت)، مما يعني أنه يجب طهي الطعام لفترة أطول.
التأثير الأكثر دقة على نقطة الانصهار
من الصلب إلى السائل: تغير صغير في الحجم
على عكس الغليان، يكون التغير في الحجم أثناء الانصهار صغيرًا جدًا. عادة ما تكون كثافات المادة في شكلها الصلب والسائل متشابهة جدًا.
نظرًا لأن التغير في الحجم ضئيل، فإن للضغط تأثيرًا أقل دراماتيكية بكثير على نقطة الانصهار.
بالنسبة لمعظم المواد: زيادة الضغط ترفع نقطة الانصهار
معظم المواد - من المعادن إلى الشموع إلى ثاني أكسيد الكربون - تكون أكثر كثافة في شكلها الصلب منها في شكلها السائل.
في هذه الحالات، تفضل زيادة الضغط الطور الصلب الأكثر تماسكًا. هذا يجعل الانصهار أكثر صعوبة قليلاً، لذلك يلزم درجة حرارة أعلى. ترتفع نقطة الانصهار مع الضغط.
شذوذ الماء: استثناء حاسم
الماء استثناء رائع ونادر. الماء الصلب (الجليد) أقل كثافة من الماء السائل، وهذا هو السبب في أن الجليد يطفو.
نظرًا لأن الماء السائل هو الطور الأكثر كثافة، فإن زيادة الضغط على الجليد تفضل تكوين السائل. هذا يعني أنه تحت الضغط العالي، سيذوب الجليد عند درجة حرارة أقل من 0 درجة مئوية (32 درجة فهرنهايت).
مثال واقعي: شفرة متزلج الجليد
التوضيح الكلاسيكي لهذا المبدأ هو متزلج الجليد. تركز الشفرة الرفيعة للمزلج وزن المتزلج بالكامل على منطقة صغيرة جدًا، مما يخلق ضغطًا هائلاً على الجليد.
يتسبب هذا الضغط العالي في ذوبان الجليد الموجود مباشرة تحت الشفرة عند درجة حرارة أقل قليلاً، مما يخلق طبقة مجهرية من الماء تعمل على تليين مسار الشفرة.
فهم المقايضات: التصور باستخدام مخطط الطور
مخطط الطور هو خريطة بسيطة توضح حالة المادة (صلبة أو سائلة أو غازية) عند أي مزيج من درجة الحرارة والضغط.
الحد الفاصل بين السائل والغاز
الخط الفاصل بين الطورين السائل والغازي دائمًا ما يميل لأعلى وإلى اليمين. يؤكد هذا بصريًا أنه كلما زدت الضغط (بالتحرك لأعلى على المحور الرأسي)، يجب عليك أيضًا زيادة درجة الحرارة (بالتحرك يمينًا على المحور الأفقي) لجعل المادة تغلي.
الحد الفاصل بين الصلب والسائل
الخط الفاصل بين الطورين الصلب والسائل عمودي تقريبًا، مما يدل على أن للضغط تأثيرًا أصغر بكثير على الانصهار.
بالنسبة لمعظم المواد، يميل هذا الخط قليلاً إلى اليمين (ضغط أعلى، نقطة انصهار أعلى). بالنسبة للماء، يميل هذا الخط بشكل فريد إلى اليسار، مما يدل على أن الضغط العالي يؤدي إلى نقطة انصهار أقل.
مبادئ أساسية للتطبيق العملي
لتطبيق هذه المعرفة بفعالية، ركز على المادة ونوع تغير الطور المعني.
- إذا كنت تتعامل مع الغليان أو التكثف: تذكر أن الضغط هو العامل المهيمن. الضغط الأعلى يعني نقطة غليان أعلى، والضغط الأقل يعني نقطة غليان أقل.
- إذا كنت تتعامل مع الانصهار أو التجمد (لمعظم المواد): تأثير الضغط ضئيل. الضغط الأعلى سيزيد نقطة الانصهار قليلاً عن طريق تفضيل الحالة الصلبة الأكثر كثافة.
- إذا كنت تتعامل خصيصًا مع جليد الماء: تذكر أنه استثناء. الضغط الأعلى يخفض نقطة التجمد/الانصهار عن طريق تفضيل الحالة السائلة الأكثر كثافة.
يمنحك فهم كيفية تفاعل الضغط ودرجة الحرارة تحكمًا مباشرًا في الحالة الفيزيائية للمادة.
جدول الملخص:
| تغير الطور | تأثير زيادة الضغط | المبدأ الأساسي | مثال شائع |
|---|---|---|---|
| الغليان | يرفع نقطة الغليان | يفضل الطور الأكثر كثافة (السائل) | قدر الضغط (يغلي الماء >100 درجة مئوية) |
| الانصهار (معظم المواد) | يرفع نقطة الانصهار قليلاً | يفضل الطور الصلب الأكثر كثافة | المعادن تحت ضغط عالٍ |
| الانصهار (الماء/الجليد) | يخفض نقطة الانصهار | يفضل الطور السائل الأكثر كثافة | التزلج على الجليد (الضغط يذيب الجليد) |
هل تحتاج إلى تحكم دقيق في تغيرات الطور في عملياتك المختبرية؟ تتخصص KINTEK في معدات الضغط العالي ودرجة الحرارة لتطبيقات المختبرات. سواء كنت تقوم بتطوير مواد جديدة، أو إجراء تركيب كيميائي، أو دراسة سلوك الطور، فإن مفاعلاتنا وأفراننا توفر التحكم الدقيق في الضغط ودرجة الحرارة الذي تحتاجه. اتصل بخبرائنا اليوم لمناقشة كيف يمكن لحلولنا تعزيز كفاءة ودقة بحثك.
دليل مرئي