لا، الجرافيت ليس معدنًا، ولكنه موصل ممتاز للكهرباء. هذا التمييز هو مصدر للارتباك المتكرر، حيث غالبًا ما نتعلم ربط التوصيل حصريًا بالعناصر المعدنية. الجرافيت هو متآصل—شكل هيكلي محدد—لعنصر الكربون اللافلزي.
السبب الأساسي لهذا الارتباك هو أننا نميل إلى تجميع المواد حسب فئات بسيطة بدلاً من تركيبتها الأساسية. الجرافيت، على الرغم من كونه لافلزًا، يوصل الكهرباء لأن ترتيبه الذري الطبقي الفريد يخلق إلكترونات "حرة" تتصرف تمامًا مثل الإلكترونات في معدن حقيقي.

ما هو الجرافيت؟ شكل فريد من الكربون
تنشأ خصائص الجرافيت مباشرة من تركيبته الذرية الفريدة. فهم هذه التركيبة هو المفتاح لفهم سلوكه.
ليس معدنًا، بل متآصل
يمكن للعناصر أن توجد في أشكال فيزيائية مختلفة تسمى المتآصلات. هذه الأشكال لها نفس الذرات ولكن ترتيبات هيكلية مختلفة، مما يمنحها خصائص متباينة بشكل كبير.
الجرافيت هو متآصل من الكربون. أشهر متآصل آخر للكربون هو الماس. على الرغم من أن كلاهما كربون نقي، إلا أن تركيباتهما تجعل الجرافيت موصلًا ناعمًا والماس عازلًا صلبًا.
تركيبة من طبقات متراصة
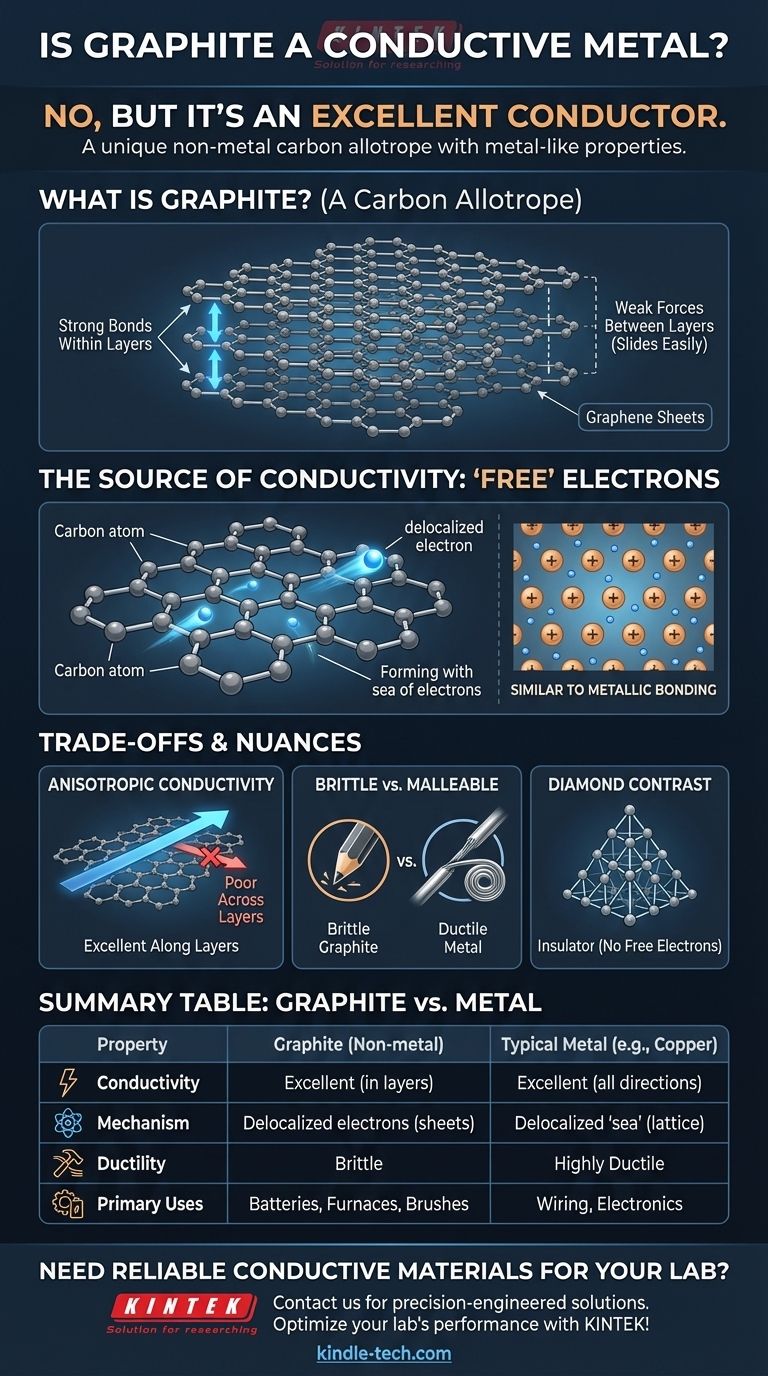
يتكون الجرافيت من عدد لا يحصى من الصفائح المسطحة المتراصة فوق بعضها البعض. كل صفيحة، تُعرف باسم الجرافين، هي طبقة بسمك ذرة واحدة من ذرات الكربون مرتبة في شبكة سداسية تشبه قرص العسل.
الروابط التي تربط الذرات داخل الصفيحة قوية بشكل لا يصدق. ومع ذلك، فإن القوى التي تربط الصفائح المختلفة ببعضها البعض ضعيفة جدًا، مما يسمح لها بالانزلاق بسهولة. هذا هو السبب في أن الجرافيت ناعم ومتقشر، ويشكل "الرصاص" في أقلام الرصاص.
مصدر توصيل الجرافيت
يكمن سبب توصيل الجرافيت للكهرباء في كيفية مشاركة إلكتروناته—أو بالأحرى، عدم مشاركتها. هذا يحاكي آلية التوصيل في المعادن دون أن يكون الجرافيت معدنًا في حد ذاته.
دور إلكترونات الكربون
تحتوي كل ذرة كربون على أربعة إلكترونات خارجية (إلكترونات التكافؤ) متاحة للترابط. في التركيبة السداسية لورقة الجرافين، تشكل كل ذرة كربون روابط تساهمية قوية مع ثلاث ذرات مجاورة.
الإلكترون "الحر" غير المتمركز
هذا يترك أحد إلكترونات التكافؤ الأربعة غير مرتبط. هذا الإلكترون الرابع ليس محبوسًا في رابطة بين ذرتين محددتين. بدلاً من ذلك، يصبح غير متمركز، حرًا في التحرك في أي مكان على طول ورقة الجرافين ثنائية الأبعاد.
"بحر من الإلكترونات" في لافلز
تشكل هذه المجموعة من الإلكترونات غير المتمركزة "بحرًا متحركًا من الإلكترونات" داخل كل طبقة. وبما أن التيار الكهربائي هو ببساطة تدفق الإلكترونات، فإن هذه الإلكترونات الحرة الحركة تسمح للجرافيت بتوصيل الكهرباء بسهولة.
هذا مشابه بشكل أساسي للترابط المعدني، حيث توجد شبكة من أيونات المعادن الموجبة في "بحر" من الإلكترونات المشتركة وغير المتمركزة. يحقق الجرافيت نتيجة مماثلة باستخدام تركيبة ذرية مختلفة تمامًا.
فهم المفاضلات والفروق الدقيقة
بينما الجرافيت موصل، فإنه ليس بديلاً مثاليًا للمعادن. طبيعته اللافلزية تأتي مع مفاضلات مميزة.
التوصيل ليس موحدًا
الجرافيت متباين الخواص بشكل كبير، مما يعني أن خصائصه تعتمد على الاتجاه. يوصل الكهرباء بشكل ممتاز على طول طبقات الجرافين، ولكنه يوصلها بشكل ضعيف جدًا عبر هذه الطبقات. معظم المعادن، على النقيض، متماثلة الخواص وتوصل الكهرباء بنفس الكفاءة في جميع الاتجاهات.
التقصف مقابل الليونة
المعادن عادة ما تكون مطيلية وقابلة للطرق، مما يعني أنه يمكن سحبها إلى أسلاك أو طرقها لتشكيل أشكال جديدة دون أن تنكسر. الجرافيت هش وسيتكسر تحت ضغط مماثل. لا يمكنك تشكيل سلك جرافيت عن طريق شده.
الماس: النظير العازل
يوفر الماس التباين المثالي. في شبكته الصلبة رباعية الأوجه، ترتبط كل ذرة كربون بأربع ذرات أخرى، مستخدمة جميع إلكترونات التكافؤ الأربعة. مع عدم وجود إلكترونات غير متمركزة، لا يوجد شيء حر للحركة وحمل التيار، مما يجعل الماس عازلًا كهربائيًا ممتازًا.
اتخاذ الخيار الصحيح لتطبيقك
يسمح لك فهم هذه المبادئ باختيار المادة الصحيحة بناءً على الخصائص المحددة المطلوبة للمهمة.
- إذا كان تركيزك الأساسي على التوصيل المرن والمتعدد الاتجاهات: تظل المعادن مثل النحاس والألومنيوم الخيار الأفضل نظرًا لليونتها وطبيعتها متماثلة الخواص.
- إذا كان تركيزك الأساسي على موصل خفيف الوزن ومستقر كيميائيًا لدرجات الحرارة العالية: الجرافيت مادة مثالية لتطبيقات مثل أقطاب البطاريات، وبطانات الأفران، وفرش المحركات الكهربائية.
- إذا كان تركيزك الأساسي على الصلابة والعزل الكهربائي: الماس، المتآصل الآخر الشهير للكربون، هو الحل، مما يثبت أن الترتيب الذري يحدد كل شيء.
في النهاية، تُعرّف خصائص المادة بتركيبتها الذرية، وليس بالفئة البسيطة التي نضعها فيها.
جدول الملخص:
| الخاصية | الجرافيت | معدن نموذجي (مثل النحاس) |
|---|---|---|
| نوع المادة | لافلز (متآصل كربون) | معدن |
| التوصيل الكهربائي | ممتاز (داخل الطبقات) | ممتاز (في جميع الاتجاهات) |
| آلية التوصيل | إلكترونات غير متمركزة في صفائح الجرافين | "بحر" من الإلكترونات غير المتمركزة |
| المطيلية/قابلية الطرق | هش، لا يمكن سحبه إلى أسلاك | مطيل وقابل للطرق بدرجة عالية |
| حالات الاستخدام الرئيسية | البطاريات، بطانات الأفران، فرش المحركات | الأسلاك، المكونات الهيكلية، الإلكترونيات |
هل تحتاج إلى مادة موصلة موثوقة لتطبيقك المختبري؟ سواء كنت تعمل مع أفران عالية الحرارة، أو أبحاث البطاريات، أو إعدادات الأقطاب الكهربائية المخصصة، فإن خبرة KINTEK في معدات المختبرات والمواد الاستهلاكية تضمن حصولك على الحل الصحيح. يمكن لفريقنا مساعدتك في اختيار المواد التي تتوافق مع متطلبات التوصيل ودرجة الحرارة والمتانة المحددة لديك. اتصل بنا اليوم لتحسين أداء مختبرك باستخدام حلول مصممة بدقة من KINTEK!
دليل مرئي
المنتجات ذات الصلة
- فرن تفحيم الجرافيت عالي الموصلية الحرارية
- قطب جرافيت قرصي وقضيبي ولوح جرافيت كهروكيميائي
- فرن تفحيم الجرافيت الفراغي فائق الحرارة
- بوتقة جرافيت نقية عالية النقاء للتبخير
- لوح كربون جرافيت مصنّع بطريقة الضغط الأيزوستاتيكي
يسأل الناس أيضًا
- ما هو العيب الرئيسي لفرن الجرافيت؟ إدارة مخاطر التفاعلية والتلوث
- ما هو النطاق الحراري لفرن الجرافيت؟ اكتشف ما يصل إلى 3000 درجة مئوية لمعالجة المواد المتقدمة.
- ما هو استخدام فرن الجرافيت؟ تحقيق معالجة بدرجة حرارة قصوى للمواد المتقدمة
- ما هي عيوب فرن الجرافيت؟ القيود الرئيسية وتكاليف التشغيل
- ما هو الغاز المستخدم في الفرن الجرافيتي؟ تحقيق أقصى قدر من الدقة باستخدام الغاز الخامل المناسب












