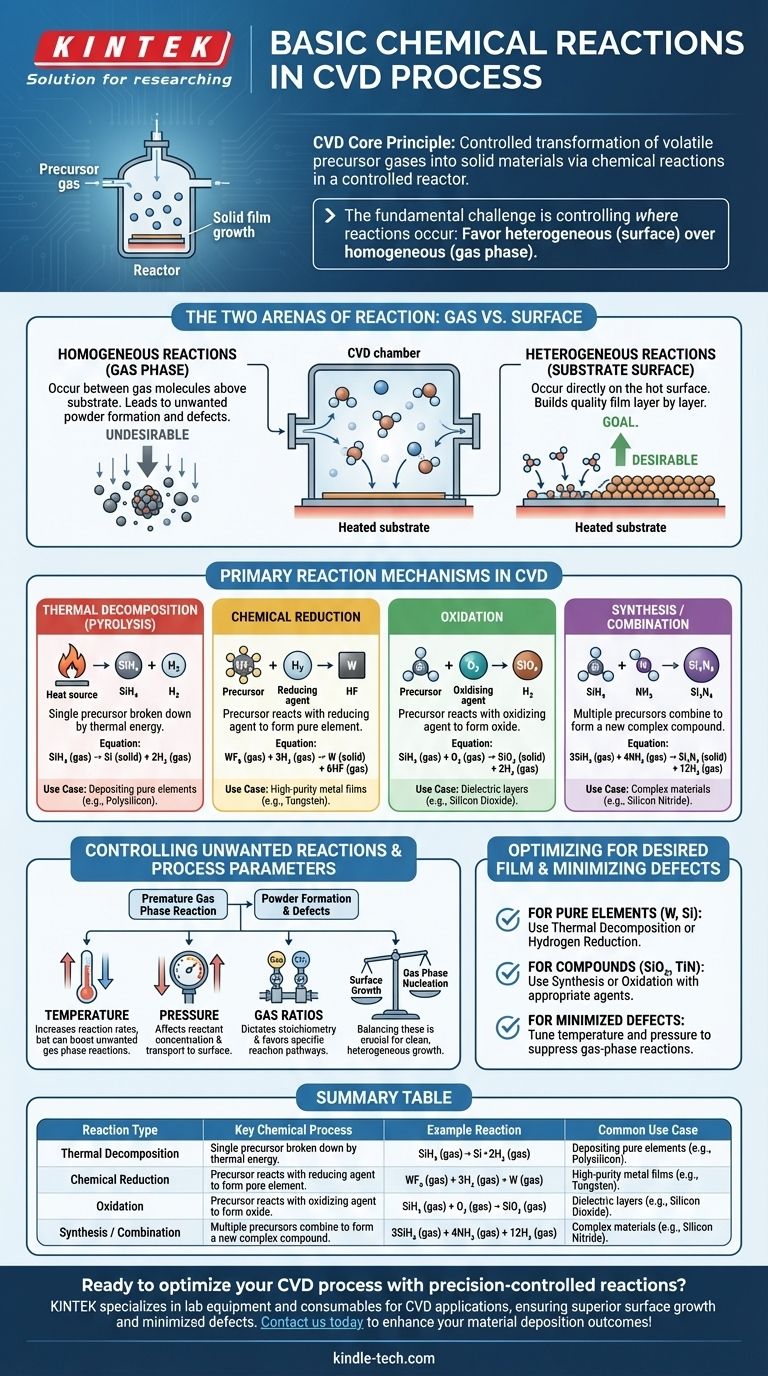
في جوهره، الترسيب الكيميائي للبخار (CVD) هو عملية تفاعلات كيميائية مضبوطة. تم تصميم هذه التفاعلات لتحويل الغازات الأولية المستقرة والمتطايرة إلى مادة صلبة غير متطايرة مباشرة على الركيزة. الآليات الأكثر شيوعًا التي تقود هذا التحول هي التحلل الحراري (التحلل الحراري)، والاختزال الكيميائي، والأكسدة، وتفاعلات التخليق، وكلها تحدث ضمن بيئة مفاعل مضبوطة للغاية.
التحدي الأساسي في أي عملية ترسيب كيميائي للبخار ليس مجرد بدء التفاعلات الكيميائية، بل التحكم بدقة في *أين* تحدث. الهدف هو تفضيل التفاعلات غير المتجانسة على سطح الركيزة لبناء غشاء عالي الجودة، مع تقليل التفاعلات المتجانسة في الطور الغازي التي تخلق جزيئات غير مرغوب فيها.

ساحتا التفاعل: الغاز مقابل السطح
يحدث كل تفاعل كيميائي في حجرة الترسيب الكيميائي للبخار في أحد المكانين. يحدد التوازن بينهما جودة وهيكل المادة النهائية.
التفاعلات المتجانسة (في الطور الغازي)
تحدث هذه التفاعلات بين جزيئات الغاز نفسها، المعلقة في الفضاء فوق الركيزة.
في حين أن بعض الكيمياء في الطور الغازي ضرورية لإنشاء أنواع وسيطة تفاعلية، فإن التفاعلات المتجانسة المفرطة غالبًا ما تكون غير مرغوب فيها. يمكن أن تؤدي إلى تكوين جزيئات صلبة أو "مساحيق" تتساقط بعد ذلك على الركيزة، مما يسبب عيوبًا ويضر بجودة الفيلم.
التفاعلات غير المتجانسة (على سطح الركيزة)
هذه هي التفاعلات التي تبني الفيلم. تحدث مباشرة على، أو في طبقة رقيقة جدًا مجاورة لسطح الركيزة الساخن.
الهدف من عملية الترسيب الكيميائي للبخار المصممة جيدًا هو زيادة معدل التفاعلات غير المتجانسة. تمتص الغازات الأولية على السطح الساخن، وتتحلل أو تتفاعل مع الأنواع الممتزة الأخرى، وتشكل الفيلم الصلب المستقر طبقة ذرية تلو الأخرى.
آليات التفاعل الأساسية في الترسيب الكيميائي للبخار
بينما تحدث في إحدى "الساحتين" المذكورتين أعلاه، يمكن تصنيف التفاعلات نفسها إلى عدة أنواع رئيسية بناءً على التحول الكيميائي المعني.
التحلل الحراري (التحلل الحراري)
هذا هو أبسط أنواع تفاعلات الترسيب الكيميائي للبخار وأكثرها شيوعًا. يتم تكسير غاز أولي واحد إلى مكوناته بواسطة الطاقة الحرارية وحدها.
توفر الحرارة من الركيزة الطاقة اللازمة لكسر الروابط الكيميائية لجزيء المادة الأولية، مما يترك العنصر الصلب المطلوب ليترسب على السطح. مثال كلاسيكي هو ترسيب البولي سيليكون من غاز السيلان.
SiH₄ (غاز) → Si (صلب) + 2H₂ (غاز)
الاختزال الكيميائي
في هذه العملية، يتفاعل غاز أولي (غالبًا هاليد معدني) مع عامل مختزل، عادةً الهيدروجين (H₂)، لتكوين غشاء عنصري نقي.
هذه طريقة شائعة لترسيب أغشية معدنية عالية النقاء مثل التنغستن. يقوم الهيدروجين بإزالة ذرات الهالوجين من المادة الأولية المعدنية، مما يسمح بترسيب المعدن النقي.
WF₆ (غاز) + 3H₂ (غاز) → W (صلب) + 6HF (غاز)
الأكسدة
يتضمن هذا التفاعل تفاعل غاز أولي مع عامل مؤكسد، مثل الأكسجين (O₂) أو أكسيد النيتروز (N₂O)، أو البخار (H₂O)، لتكوين غشاء أكسيد صلب.
هذه هي العملية الأساسية لإنشاء طبقات عازلة عازلة مثل ثاني أكسيد السيليكون (SiO₂)، وهو مكون حاسم في جميع الإلكترونيات الدقيقة الحديثة تقريبًا.
SiH₄ (غاز) + O₂ (غاز) → SiO₂ (صلب) + 2H₂ (غاز)
التخليق أو التوليف
هنا، يتم إدخال غازين أوليين أو أكثر للجمع وتكوين مادة مركبة جديدة على الركيزة. يتيح هذا إنشاء مواد معقدة لا يمكن تكوينها عن طريق التحلل البسيط.
على سبيل المثال، يتم تكوين نيتريد السيليكون (Si₃N₄)، وهو مادة صلبة ومقاومة كيميائيًا، عن طريق تفاعل مصدر للسيليكون مع مصدر للنيتروجين، مثل الأمونيا.
3SiH₄ (غاز) + 4NH₃ (غاز) → Si₃N₄ (صلب) + 12H₂ (غاز)
فهم المفاضلات: التحكم في التفاعلات غير المرغوب فيها
يعتمد نجاح عملية الترسيب الكيميائي للبخار بالكامل على التحكم في بيئة التفاعل لتفضيل مسارات التفاعل المرغوبة.
مشكلة تكوين المسحوق
العقبة الرئيسية في الترسيب الكيميائي للبخار هي التبلور غير المقصود في الطور الغازي. إذا كانت درجة حرارة المفاعل عالية جدًا أو كان الضغط كبيرًا جدًا، يمكن أن تتفاعل الغازات الأولية بشكل سابق لأوانه في الطور الغازي (تفاعل متجانس) قبل أن تصل إلى الركيزة. يؤدي هذا إلى إنشاء جزيئات يمكن أن تسبب عيوبًا أو تشكل فيلمًا مسحوقيًا منخفض الكثافة بدلاً من فيلم كثيف عالي الجودة.
دور معلمات العملية
يستخدم المهندسون العديد من المعلمات الرئيسية كرافعات للتحكم في حركية التفاعل وموقعه:
- درجة الحرارة: تزيد من معدلات التفاعل ولكن يمكن أن تزيد أيضًا من التفاعلات الغازية غير المرغوب فيها.
- الضغط: يؤثر على تركيز المواد المتفاعلة وكيفية سفرها بسرعة إلى السطح.
- نسب الغازات: تحدد التكافؤ وتتحكم في مسار التفاعل المفضل.
يعد موازنة هذه العوامل أمرًا بالغ الأهمية لتعزيز النمو النظيف وغير المتجانس على سطح الركيزة.
تحسين التفاعلات للفيلم المطلوب
يتم تحديد مسار التفاعل الكيميائي المحدد الذي تستخدمه بالكامل من خلال المادة التي تنوي إنشائها.
- إذا كان تركيزك الأساسي هو ترسيب عنصر نقي (مثل التنغستن، السيليكون): فمن المرجح أن تعتمد على التحلل الحراري أو تفاعل اختزال الهيدروجين باستخدام مادة أولية واحدة وربما عامل مختزل.
- إذا كان تركيزك الأساسي هو إنشاء أكسيد أو نيتريد مركب (مثل SiO₂، TiN): فستستخدم تفاعل تخليق أو أكسدة، وإدخال عامل مؤكسد أو عامل نيترة إلى جانب المادة الأولية الرئيسية.
- إذا كان تركيزك الأساسي هو تقليل العيوب وتحقيق فيلم عالي الجودة: فإن مهمتك الرئيسية هي ضبط درجة الحرارة والضغط لقمع التفاعلات المتجانسة في الطور الغازي وتعزيز النمو النظيف وغير المتجانس على الركيزة.
في نهاية المطاف، إتقان الترسيب الكيميائي للبخار هو إتقان فن توجيه الكيمياء لتحدث في وقت ومكان محددين.
جدول ملخص:
| نوع التفاعل | العملية الكيميائية الرئيسية | مثال التفاعل | حالة الاستخدام الشائعة |
|---|---|---|---|
| التحلل الحراري (التحلل الحراري) | تتحلل مادة أولية واحدة عن طريق الحرارة | SiH₄ (غاز) → Si (صلب) + 2H₂ (غاز) | ترسيب عناصر نقية مثل البولي سيليكون |
| الاختزال الكيميائي | تتفاعل المادة الأولية مع عامل مختزل (مثل H₂) | WF₆ (غاز) + 3H₂ (غاز) → W (صلب) + 6HF (غاز) | أغشية معدنية عالية النقاء (مثل التنغستن) |
| الأكسدة | تتفاعل المادة الأولية مع عامل مؤكسد (مثل O₂) | SiH₄ (غاز) + O₂ (غاز) → SiO₂ (صلب) + 2H₂ (غاز) | طبقات عازلة مثل ثاني أكسيد السيليكون |
| التخليق/التوليف | تتحد مواد أولية متعددة لتكوين مركب | 3SiH₄ (غاز) + 4NH₃ (غاز) → Si₃N₄ (صلب) + 12H₂ (غاز) | مواد معقدة مثل نيتريد السيليكون |
هل أنت مستعد لتحسين عملية الترسيب الكيميائي للبخار لديك بتفاعلات مضبوطة بدقة؟ تتخصص KINTEK في معدات المختبرات والمواد الاستهلاكية لتطبيقات الترسيب الكيميائي للبخار، مما يساعدك على تحقيق أغشية رقيقة خالية من العيوب من خلال حلول المفاعلات المصممة خصيصًا. سواء كنت ترسب معادن أو أكاسيد أو نيتريدات، فإن خبرتنا تضمن نموًا سطحيًا فائقًا وتقليلًا لعيوب الطور الغازي. اتصل بنا اليوم لمناقشة كيف يمكن لأنظمة الترسيب الكيميائي للبخار لدينا تعزيز نتائج ترسيب المواد لديك!
دليل مرئي
المنتجات ذات الصلة
- نظام معدات ترسيب البخار الكيميائي متعدد الاستخدامات ذو الأنبوب الحراري المصنوع حسب الطلب للعملاء
- نظام معدات الترسيب الكيميائي للبخار (CVD) - فرن أنبوبي PECVD منزلق مع جهاز تغويز السوائل - ماكينة PECVD
- ألماس CVD لتطبيقات الإدارة الحرارية
- نظام معدات آلة HFCVD لطلاء النانو الماسي لقوالب السحب
- طلاء الألماس المخصص بتقنية الترسيب الكيميائي للبخار (CVD) للتطبيقات المخبرية
يسأل الناس أيضًا
- ما هو التخليق والآلية المتضمنة في تحضير أنابيب الكربون النانوية باستخدام عملية الترسيب الكيميائي للبخار (CVD)؟ تحكم في النمو ليتناسب مع تطبيقك
- ما هي وظيفة فرن الأنبوب CVD عالي الحرارة في تحضير رغوة الجرافين ثلاثية الأبعاد؟ إتقان نمو المواد النانوية ثلاثية الأبعاد
- كيف يمنع فرن الأنبوب CVD تلبد الدعامات الفضية؟ تعزيز متانة الغشاء وأدائه
- ما هي وظيفة الفرن الأنبوبي في تصنيع كربيد السيليكون بواسطة الترسيب الكيميائي للبخار؟ تحقيق مساحيق كربيد السيليكون فائقة النقاء
- ما هي الطريقة المستخدمة لنمو الجرافين؟ إتقان الإنتاج عالي الجودة باستخدام الترسيب الكيميائي للبخار (CVD)