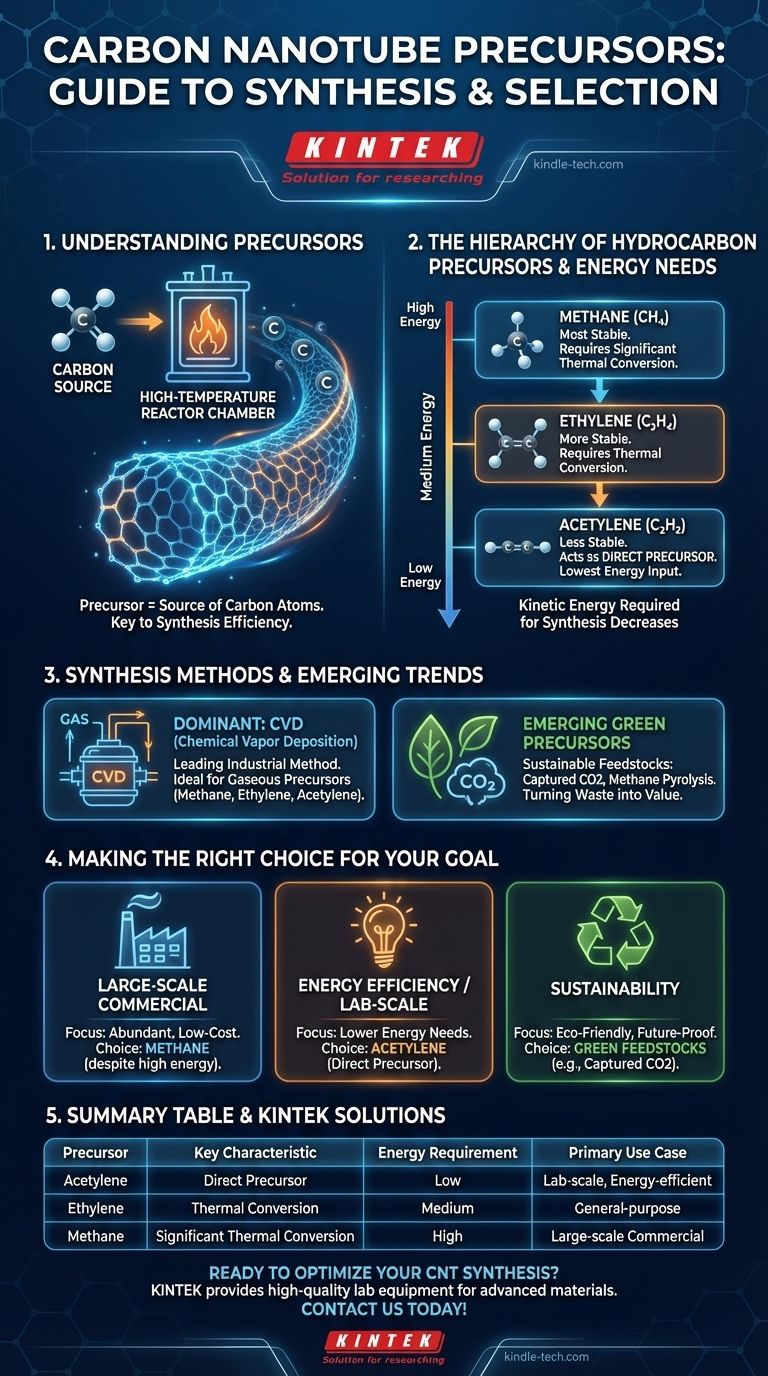
السلائف الأكثر شيوعًا للأنابيب النانوية الكربونية (CNTs) هي غازات الهيدروكربون البسيطة. يعمل الميثان والإيثيلين، وخاصة الأسيتيلين، كمصدر مباشر لذرات الكربون التي تتجمع لتشكيل بنية الأنابيب النانوية أثناء التخليق.
يعد اختيار سلف الكربون قرارًا حاسمًا يؤثر بشكل مباشر على متطلبات الطاقة والكفاءة الكلية لعملية التخليق بأكملها، حيث تتطلب الجزيئات الأبسط غالبًا المزيد من الطاقة لتفكيكها.

فهم السلائف وظروف العملية
السلف هو المادة الخام الأساسية التي توفر العناصر الضرورية للتخليق الكيميائي. بالنسبة للأنابيب النانوية الكربونية، فإن السلف هو ببساطة مصدر ذرات الكربون.
دور مصدر الكربون
يتم إدخال غاز السلف في مفاعل عالي الحرارة، حيث يتحلل. هذه العملية، التي غالبًا ما تساعدها محفزات معدنية، تحرر ذرات الكربون لتتجمع ذاتيًا في البنية الشبكية السداسية الفريدة للأنبوب النانوي.
معلمات التخليق الرئيسية
يعتمد نجاح هذا التحويل على توازن دقيق بين معلمات التشغيل. تعد درجة الحرارة وتركيز مصدر الكربون وزمن المكوث (مدة بقاء الغاز في المفاعل) هي العوامل الثلاثة الأكثر أهمية التي تحدد كفاءة إنتاج الأنابيب النانوية الكربونية.
التسلسل الهرمي لسلائف الهيدروكربون الشائعة
لا تتصرف جميع سلائف الهيدروكربون بنفس الطريقة. تحدد استقرارها الكيميائي كمية الطاقة المطلوبة لبدء عملية نمو الأنابيب النانوية الكربونية.
الأسيتيلين: السلف المباشر
الأسيتيلين فريد من نوعه لأنه يمكن أن يعمل كسلف مباشر للأنابيب النانوية الكربونية. بنيته الكيميائية أقل استقرارًا، مما يسمح له بالتحلل وتوفير ذرات الكربون دون الحاجة إلى مدخلات طاقة إضافية كبيرة للتحويل الحراري.
الميثان والإيثيلين: يتطلبان تحويلًا حراريًا
على النقيض من ذلك، فإن الميثان والإيثيلين جزيئات أكثر استقرارًا. تعتمد على عمليات التحويل الحراري، مما يعني أنها تتطلب كمية كبيرة من الطاقة لكسر روابطها الكيميائية قبل أن تصبح ذرات الكربون متاحة لتخليق الأنابيب النانوية الكربونية.
مقياس متطلبات الطاقة
يخلق هذا تسلسلًا هرميًا واضحًا للطاقة بين السلائف الشائعة. تتبع الطاقة الحركية اللازمة للتخليق الناجح هذا الترتيب:
الميثان > الإيثيلين > الأسيتيلين
الميثان، كونه الأكثر استقرارًا، يتطلب أكبر قدر من الطاقة للتحلل، بينما يتطلب الأسيتيلين الأقل.
كيف تؤثر طرق التخليق على اختيار السلف
بينما توجد طرق أقدم، فإن العملية التجارية السائدة لصنع الأنابيب النانوية الكربونية اليوم تؤثر بشكل كبير على السلائف المستخدمة.
الترسيب الكيميائي للبخار (CVD)
يعد الترسيب الكيميائي للبخار (CVD) الطريقة الصناعية الرائدة لإنتاج الأنابيب النانوية الكربونية. هذه العملية مناسبة تمامًا للسلائف الغازية مثل الميثان والإيثيلين والأسيتيلين، مما يجعلها أساس الصناعة.
الأساليب القديمة
تعد الطرق التقليدية مثل الاستئصال بالليزر والتفريغ القوسي، والتي تتضمن تبخير هدف كربوني صلب، أقل شيوعًا للإنتاج على نطاق واسع اليوم مقارنة بنهج CVD الأكثر قابلية للتوسع.
السلائف الخضراء الناشئة
يبحث البحث بنشاط عن مواد أولية أكثر استدامة. تهدف هذه الطرق الناشئة إلى إنشاء أنابيب نانوية كربونية من النفايات أو الكربون المحتجز، مما يمثل تحولًا كبيرًا عن مصادر الهيدروكربون التقليدية. ويشمل ذلك استخدام ثاني أكسيد الكربون المحتجز عن طريق التحليل الكهربائي أو الاستفادة من الانحلال الحراري للميثان.
اتخاذ الخيار الصحيح لهدفك
يعتمد السلف المثالي كليًا على الهدف الأساسي للتخليق.
- إذا كان تركيزك الأساسي هو الإنتاج التجاري على نطاق واسع: غالبًا ما يتم اختيار المواد الأولية الوفيرة ومنخفضة التكلفة مثل الميثان، على الرغم من متطلباتها العالية من الطاقة.
- إذا كان تركيزك الأساسي هو كفاءة الطاقة أو التخليق على نطاق المختبر: يعتبر الأسيتيلين مرشحًا قويًا نظرًا لقدرته على العمل كسلف مباشر باحتياجات طاقة أقل.
- إذا كان تركيزك الأساسي هو الاستدامة: فإن المواد الأولية الخضراء الناشئة مثل ثاني أكسيد الكربون المحتجز أو الميثان المتحلل حراريًا هي المستقبل، حيث تحول مجاري النفايات إلى مواد عالية القيمة.
في النهاية، يحدد اختيار سلف الكربون بشكل أساسي التكلفة والكفاءة والتأثير البيئي لتخليق الأنابيب النانوية الكربونية.
جدول ملخص:
| السلف | الخاصية الرئيسية | متطلبات الطاقة | حالة الاستخدام الأساسية |
|---|---|---|---|
| الأسيتيلين | يعمل كسلف مباشر | منخفضة | تخليق على نطاق المختبر، موفر للطاقة |
| الإيثيلين | يتطلب تحويلًا حراريًا | متوسطة | إنتاج للأغراض العامة |
| الميثان | يتطلب تحويلًا حراريًا كبيرًا | عالية | إنتاج تجاري على نطاق واسع |
هل أنت مستعد لتحسين تخليق الأنابيب النانوية الكربونية لديك؟
يعد اختيار السلف المناسب أمرًا بالغ الأهمية لتحقيق الجودة والإنتاجية وفعالية التكلفة المطلوبة في إنتاج الأنابيب النانوية الكربونية. تتخصص KINTEK في توفير معدات ومواد استهلاكية مخبرية عالية الجودة مصممة خصيصًا لتخليق المواد المتقدمة، بما في ذلك الأنابيب النانوية الكربونية.
يمكن لخبرائنا مساعدتك في اختيار الأدوات المناسبة وتقديم رؤى لتوسيع نطاق عمليتك بفعالية. تواصل معنا اليوم لمناقشة احتياجاتك المحددة ودع KINTEK تكون شريكك في الابتكار.
دليل مرئي