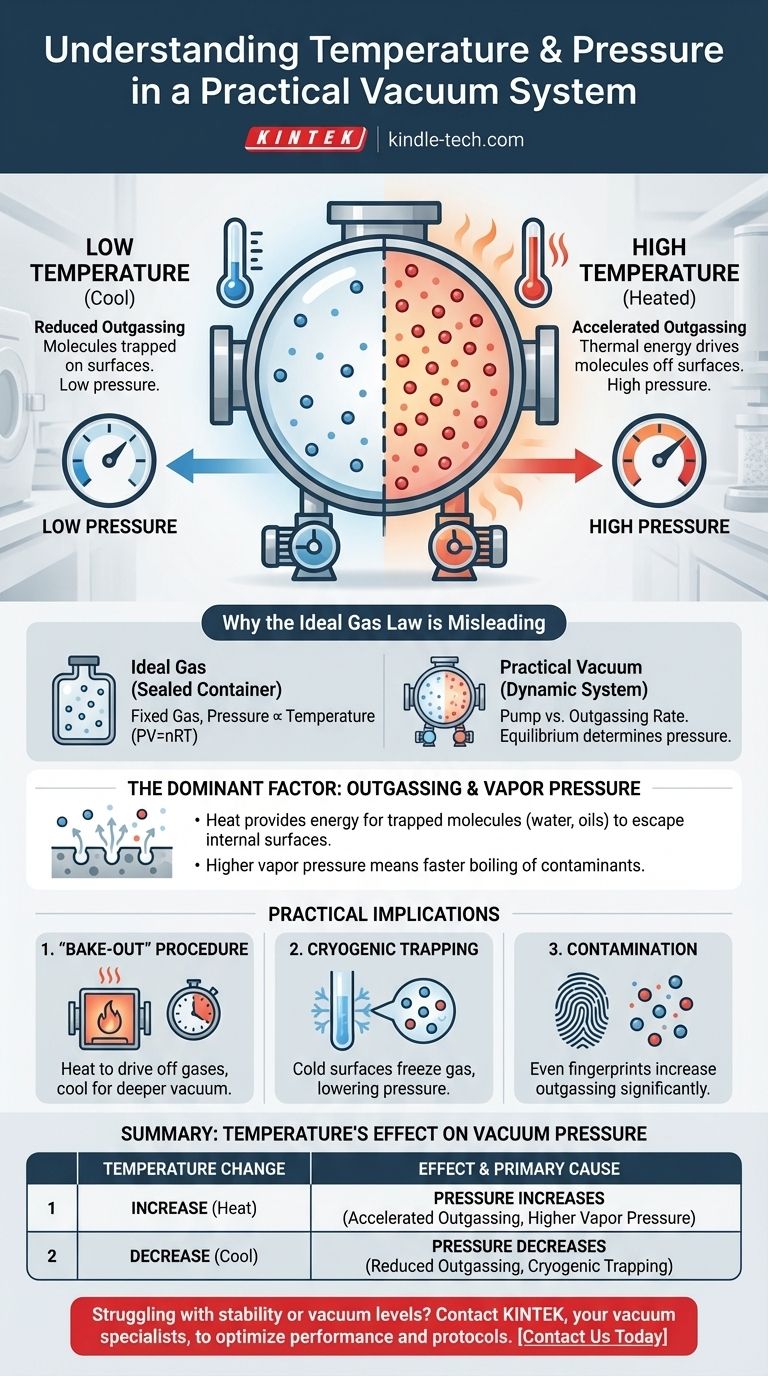
في نظام فراغ عملي، العلاقة مباشرة: زيادة درجة حرارة النظام ستزيد الضغط، وبالتالي تقلل من جودة الفراغ. يحدث هذا لأن الحرارة توفر الطاقة للجزيئات المحتجزة على الأسطح الداخلية للغرفة للهروب إلى الفراغ. هذه العملية، المعروفة باسم إطلاق الغازات (outgassing)، هي المصدر المهيمن للضغط في بيئات الفراغ العالي.
لا يحكم الضغط داخل غرفة فراغ حقيقية قانون الغاز المثالي، بل يحكمه معدل إطلاق الغازات من أسطحها الداخلية. تزيد درجات الحرارة المرتفعة هذا المعدل، مما يطلق المزيد من جزيئات الغاز وبالتالي يزيد الضغط الكلي.

لماذا يعتبر قانون الغاز المثالي مضللاً هنا
مفهوم خاطئ لـ "غاز محتوي"
يصف قانون الغاز المثالي المعروف (PV=nRT) العلاقة بين الضغط والحجم ودرجة الحرارة لكمية ثابتة من الغاز في وعاء محكم الإغلاق. في هذا السيناريو، يتناسب الضغط طرديًا مع درجة الحرارة.
ومع ذلك، فإن غرفة الفراغ ليست وعاءً محكم الإغلاق بكمية ثابتة من الغاز. إنها نظام ديناميكي حيث تقوم مضخة بإزالة الجزيئات بنشاط.
الواقع: توازن ديناميكي
يتم تحديد الضغط في الفراغ من خلال التوازن بين المعدل الذي تزيل به المضخة الجزيئات والمعدل الذي تدخل به جزيئات جديدة إلى النظام. المصدر الأساسي لهذه الجزيئات الجديدة هو الأسطح الداخلية للغرفة نفسها.
العامل المهيمن: إطلاق الغازات وضغط البخار
ما هو إطلاق الغازات؟
تحتوي جميع المواد على جزيئات غاز ممتزة (ملتصقة بالسطح) أو ممتصة (محاصرة داخل المادة). في الفراغ، ستتطاير هذه الجزيئات تدريجيًا من الأسطح.
تسمى هذه العملية إطلاق الغازات (outgassing). المسبب الرئيسي في معظم أنظمة الفراغ هو بخار الماء، ولكن الزيوت والمذيبات والغازات المحتجزة أثناء التصنيع تساهم أيضًا.
كيف تؤثر درجة الحرارة على إطلاق الغازات
تسخين جدران غرفة الفراغ ينقل الطاقة الحرارية إلى الجزيئات المحتجزة. تتيح هذه الطاقة المتزايدة لها التغلب على القوى التي تربطها بالسطح، مما يؤدي إلى إطلاقها في الفراغ.
درجة حرارة أعلى تعني معدل إطلاق غازات أعلى بكثير، مما يؤدي مباشرة إلى ضغط أعلى.
دور ضغط البخار
لأي مادة مكثفة، مثل قطرة ماء أو طبقة زيت داخل الغرفة، يوجد ضغط بخار. هذا هو الضغط الذي تكون عنده المادة في حالة توازن مع غازها الخاص عند درجة حرارة معينة.
مع ارتفاع درجة الحرارة، يرتفع ضغط بخار هذه الملوثات بشكل كبير. إذا تجاوز ضغط بخار الملوث الضغط في الغرفة، فسوف يغلي بسرعة، مما يتسبب في زيادة كبيرة في الضغط.
فهم الآثار العملية
إجراء "الخبز" (Bake-Out)
يستغل المهندسون هذه العلاقة بين درجة الحرارة والضغط لتحقيق فراغ فائق الارتفاع (UHV). يتم تسخين النظام، غالبًا إلى مئات الدرجات المئوية، لعدة ساعات أو أيام بينما تعمل المضخات.
يعمل هذا "الخبز" على تسريع إطلاق الغازات بشكل كبير، مما يؤدي إلى إزالة الماء المحتجز والملوثات الأخرى حتى تتمكن المضخات من إزالتها بشكل دائم. بعد تبريد النظام مرة أخرى، يكون معدل إطلاق الغازات أقل بكثير، مما يسمح بفراغ أعمق بكثير.
تأثير التبريد العميق (Cryogenics)
يتم استخدام التأثير المعاكس أيضًا. تعمل الأسطح شديدة البرودة، المعروفة باسم المصائد المبردة أو المضخات المبردة، كمصارف لجزيئات الغاز.
عندما يصطدم جزيء مثل الماء بسطح شديد البرودة، فإنه يتجمد على الفور ويصبح ضغط بخاره ضئيلًا. هذا يزيله بشكل فعال من الفراغ، مما يقلل بشكل كبير من ضغط النظام.
مشكلة التلوث
يبرز هذا المبدأ سبب أهمية النظافة القصوى في تكنولوجيا الفراغ. تحتوي بصمة الإصبع الواحدة على زيوت وماء ستعمل كمصدر كبير لإطلاق الغازات، مما يحد من الضغط الأقصى الذي يمكن أن يحققه النظام، خاصة عند تسخينه.
اتخاذ الخيار الصحيح لهدفك
لإدارة نظام الفراغ بفعالية، يجب عليك التعامل مع درجة الحرارة كمتغير تحكم أساسي.
- إذا كان تركيزك الأساسي هو تحقيق أعمق فراغ ممكن: يجب عليك تسخين الغرفة في عملية "خبز" أثناء الضخ لإخراج الغازات المحتجزة، ثم السماح لها بالتبريد لتحقيق الضغط المستهدف.
- إذا كان تركيزك الأساسي هو الحفاظ على فراغ مستقر أثناء العملية: يجب عليك ضمان التحكم الدقيق في درجة الحرارة، حيث أن حتى التقلبات الحرارية الصغيرة ستتسبب في تغيرات في الضغط بسبب تغير معدلات إطلاق الغازات.
- إذا كان تركيزك الأساسي هو التعامل مع المواد ذات ضغط البخار العالي: قد تحتاج إلى استخدام التبريد العميق (المصائد الباردة) لالتقاط الأبخرة ومنعها من إغراق مضخاتك.
في النهاية، إتقان الضغط في نظام الفراغ الخاص بك يعني إتقان الطاقة الحرارية لأسطحه.
جدول ملخص:
| تغير درجة الحرارة | التأثير على ضغط الفراغ | السبب الرئيسي |
|---|---|---|
| زيادة | يزداد الضغط | تسارع إطلاق الغازات وارتفاع ضغط بخار الملوثات. |
| نقصان | ينخفض الضغط | انخفاض معدل إطلاق الغازات؛ يمكن للأسطح المبردة أن تحبس الجزيئات. |
هل تعاني من عدم استقرار الضغط أو عدم القدرة على تحقيق مستوى الفراغ المستهدف؟ من المرجح أن تكون الإدارة الحرارية لنظامك هي المفتاح. تتخصص KINTEK في معدات المختبرات والمواد الاستهلاكية لتطبيقات الفراغ الدقيقة. يمكن لخبرائنا مساعدتك في اختيار المكونات المناسبة وتطوير بروتوكولات للخبز، أو التحكم في درجة الحرارة، أو الالتقاط المبرد لضمان أن تكون عمليات الفراغ الخاصة بك موثوقة وقابلة للتكرار. اتصل بمتخصصي الفراغ لدينا اليوم لتحسين أداء نظامك.
دليل مرئي
المنتجات ذات الصلة
- فرن صهر القوس لنظام الدوران بالصهر بالحث الفراغي
- تجميع ختم الرصاص لتمرير القطب الكهربائي بالتفريغ بشفة CF KF لأنظمة التفريغ
- مضخة تفريغ مياه متداولة للاستخدام المختبري والصناعي
- منفاخ تفريغ لتحقيق اتصال فعال وفراغ مستقر في الأنظمة عالية الأداء
- صمام كروي فراغي من الفولاذ المقاوم للصدأ 304 316 صمام توقف لأنظمة التفريغ العالي
يسأل الناس أيضًا
- ما هو الدور الأساسي الذي تلعبه أفران صهر الحث الفراغي في إنتاج الفولاذ الخالي من النيكل؟ تحقيق سبائك عالية النقاء
- ما هي الوظيفة الأساسية لفرن صهر بالحث الفراغي في تحضير سبائك النيكل-الموليبدينوم-الكروم-الحديد الرئيسية؟ ضمان نقاء عالٍ
- ما هي وظيفة فرن الصهر بالحث الفراغي؟ دليل أساسي لإنتاج سبائك FeCrAl عالية النقاء
- ما هي أنواع المعادن التي تتم معالجتها عادة في فرن صهر بالحث الفراغي؟ سبائك عالية النقاء للتطبيقات الحرجة
- ما هي مزايا فرن الصهر بالتحريض الفراغي؟ تحقيق سبائك عالية النقاء بدقة VIM



















