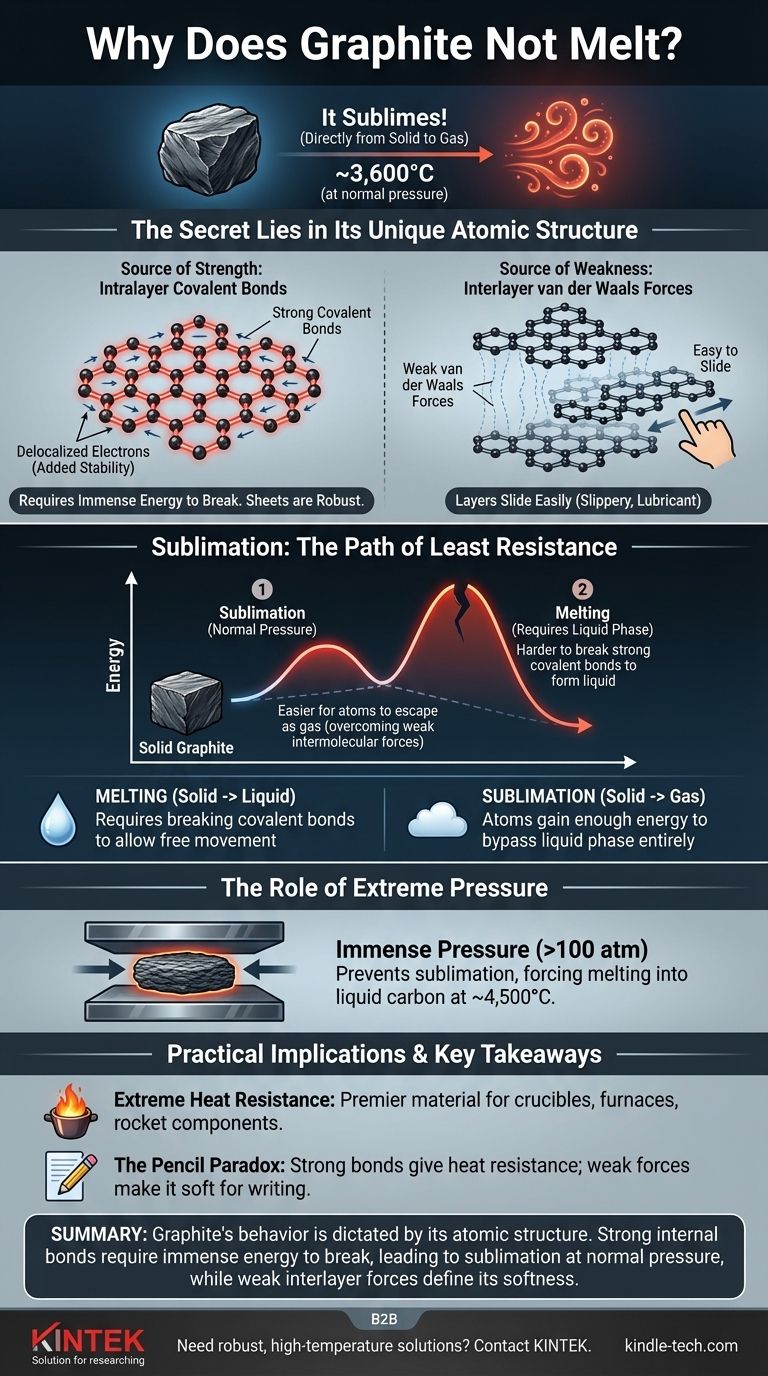
من المفاهيم الخاطئة الشائعة أن الجرافيت لا يذوب. تحت الضغط الجوي العادي، يقوم الجرافيت بشيء مختلف: يتسامى، أي يتحول مباشرة من مادة صلبة إلى غاز عند درجة حرارة عالية بشكل لا يصدق تبلغ حوالي 3600 درجة مئوية (6500 درجة فهرنهايت). هذا السلوك هو نتيجة مباشرة للقوة الهائلة للروابط الكيميائية التي تربط ذرات الكربون معًا.
السبب الأساسي لمقاومة الجرافيت الشديدة للحرارة هو بنيته الذرية الفريدة. يتكون من طبقات من ذرات الكربون مرتبطة ببعضها البعض بواسطة روابط تساهمية قوية بشكل استثنائي، والتي تتطلب كمية هائلة من الطاقة لكسرها والسماح للمادة بتغيير حالتها.

تفكيك البنية الذرية للجرافيت
لفهم سبب سلوك الجرافيت بهذه الطريقة، يجب أن ننظر إلى كيفية ترتيب ذرات الكربون فيه. تُعرّف بنيته بنوعين مختلفين جدًا من الروابط الكيميائية التي تعمل في نفس الوقت.
مصدر القوة: الروابط التساهمية داخل الطبقات
يتكون الجرافيت من صفائح مسطحة ثنائية الأبعاد من ذرات الكربون مرتبة في شبكة سداسية تشبه قرص العسل.
داخل كل صفيحة، ترتبط كل ذرة كربون بثلاث ذرات أخرى بواسطة روابط تساهمية قوية. هذه الروابط هي من أقوى الروابط الكيميائية في الطبيعة.
علاوة على ذلك، يصبح إلكترون واحد من كل ذرة كربون غير متمركز، مما يعني أنه حر في التحرك عبر الصفيحة بأكملها. تضيف مشاركة الإلكترونات هذه بين جميع الذرات في الطبقة استقرارًا كبيرًا وتزيد من قوة الروابط، مما يجعل الصفائح قوية بشكل لا يصدق ويصعب تفكيكها.
مصدر الضعف: القوى بين الطبقات
بينما ترتبط الذرات داخل الطبقة بقوة، فإن الطبقات نفسها ترتبط بقوى أضعف بكثير تُعرف باسم قوى فان دير فالس.
هذه القوى ضعيفة بما يكفي للسماح للطبقات بالانزلاق فوق بعضها البعض بسهولة. لهذا السبب يبدو الجرافيت زلقًا ويستخدم كمادة تشحيم وفي أقلام الرصاص—الكتابة تترك طبقات من الجرافيت على الورق.
التسامي: طريق المقاومة الأقل
الفرق الشديد بين الروابط القوية داخل الطبقات والقوى الضعيفة بين الطبقات يحدد كيفية استجابة الجرافيت للحرارة.
الذوبان مقابل التسامي
الذوبان هو عملية تحول المادة الصلبة إلى سائل. لكي يحدث هذا، يجب أن تكتسب الذرات طاقة كافية للتحرر من مواقعها الثابتة ولكنها تظل متجاذبة لبعضها البعض.
التسامي هو الانتقال المباشر من مادة صلبة إلى غاز. في هذه الحالة، تكتسب الذرات طاقة كبيرة جدًا بحيث تتجاوز المرحلة السائلة تمامًا وتتطاير في الهواء.
لماذا يتفوق التسامي تحت الضغط العادي
عند الضغط الجوي القياسي، تكون الطاقة المطلوبة لكسر الروابط التساهمية القوية داخل طبقات الجرافيت هائلة.
قبل أن يتمكن الهيكل من امتصاص طاقة كافية للذوبان في سائل، تكتسب الذرات على السطح طاقة كافية للتغلب على القوى الجزيئية الضعيفة وتتطاير ببساطة كغاز. من الأسهل من الناحية الطاقية للذرات أن تهرب مباشرة إلى الحالة الغازية بدلاً من كسر الروابط التساهمية المطلوبة لتكوين سائل.
دور الضغط الشديد
يمكن إجبار الجرافيت على الذوبان، ولكن فقط في ظل ظروف استثنائية.
عن طريق تطبيق ضغط هائل (أكثر من 100 ضعف الضغط الجوي العادي)، يمكنك منع ذرات الكربون من الهروب كغاز. في ظل هذه الظروف، سيذوب الجرافيت في كربون سائل عند درجة حرارة تقارب 4500 درجة مئوية (8132 درجة فهرنهايت).
الآثار العملية لهذه البنية
تمنح هذه البنية الفريدة ذات الروابط المزدوجة الجرافيت مجموعة من الخصائص التي تبدو متناقضة ولكنها ضرورية لتطبيقاته الصناعية.
مقاومة الحرارة الشديدة
نقطة التسامي العالية تجعل الجرافيت مادة رئيسية للبيئات ذات درجات الحرارة العالية. يستخدم في صناعة البوتقات لصهر المعادن، وبطانات الأفران، ومكونات محركات الصواريخ التي يجب أن تتحمل حرارة هائلة.
مفارقة قلم الرصاص
توضح بنية الجرافيت كيف يمكن أن يكون مقاومًا للحرارة بشكل لا يصدق وفي نفس الوقت ناعمًا بشكل مفاجئ. تأتي القوة من الروابط التساهمية داخل الطبقات، بينما تأتي النعومة وخصائص التشحيم من سهولة انزلاق هذه الطبقات فوق بعضها البعض.
النقاط الرئيسية لفهم الجرافيت
- إذا كان تركيزك الأساسي على سلوكه تحت الحرارة: تذكر أنه عند الضغط العادي، يتسامى الجرافيت مباشرة إلى غاز لأن الطاقة اللازمة لذلك أقل من الطاقة المطلوبة لكسر الروابط التساهمية وتكوين سائل.
- إذا كان تركيزك الأساسي على خصائصه الفيزيائية: المفتاح هو بنيته الطبقية. الروابط القوية داخل الطبقات توفر مقاومة للحرارة، بينما القوى الضعيفة بين الطبقات تجعله ناعمًا ومادة تشحيم فعالة.
- إذا كان تركيزك الأساسي على التعريف التقني للذوبان: يمكن للجرافيت أن يذوب بالتأكيد، ولكن فقط تحت ضغط عالٍ للغاية يمنع الذرات من التسامي أولاً.
في النهاية، سلوك الجرافيت هو مثال مثالي لكيفية تحديد البنية الذرية للمادة لخصائصها في العالم الحقيقي.
جدول الملخص:
| الخاصية | الوصف | السبب الرئيسي |
|---|---|---|
| نقطة التسامي | ~3600 درجة مئوية (عند الضغط العادي) | قوى فان دير فالس الضعيفة بين الطبقات تسمح للذرات بالهروب كغاز قبل الذوبان. |
| نقطة الانصهار | ~4500 درجة مئوية (تحت ضغط شديد >100 ضغط جوي) | الضغط العالي يمنع التسامي، مما يجبر الروابط التساهمية على الانكسار للذوبان. |
| مقاومة الحرارة | ممتاز للتطبيقات ذات درجات الحرارة العالية | الروابط التساهمية القوية للغاية داخل طبقات الكربون تتطلب طاقة هائلة لكسرها. |
هل تحتاج إلى حلول قوية وعالية الحرارة لمختبرك؟
خصائص الجرافيت الفريدة تجعله مادة أساسية للتطبيقات الصعبة. في KINTEK، نحن متخصصون في توفير معدات ومواد استهلاكية عالية الجودة للمختبرات، بما في ذلك بوتقات الجرافيت ومكونات الأفران، المصممة لتحمل الظروف القاسية.
دع خبرائنا يساعدونك في اختيار المواد المناسبة لتعزيز كفاءة وسلامة مختبرك. اتصل بـ KINTEK اليوم لمناقشة احتياجاتك المحددة لدرجات الحرارة العالية!
دليل مرئي