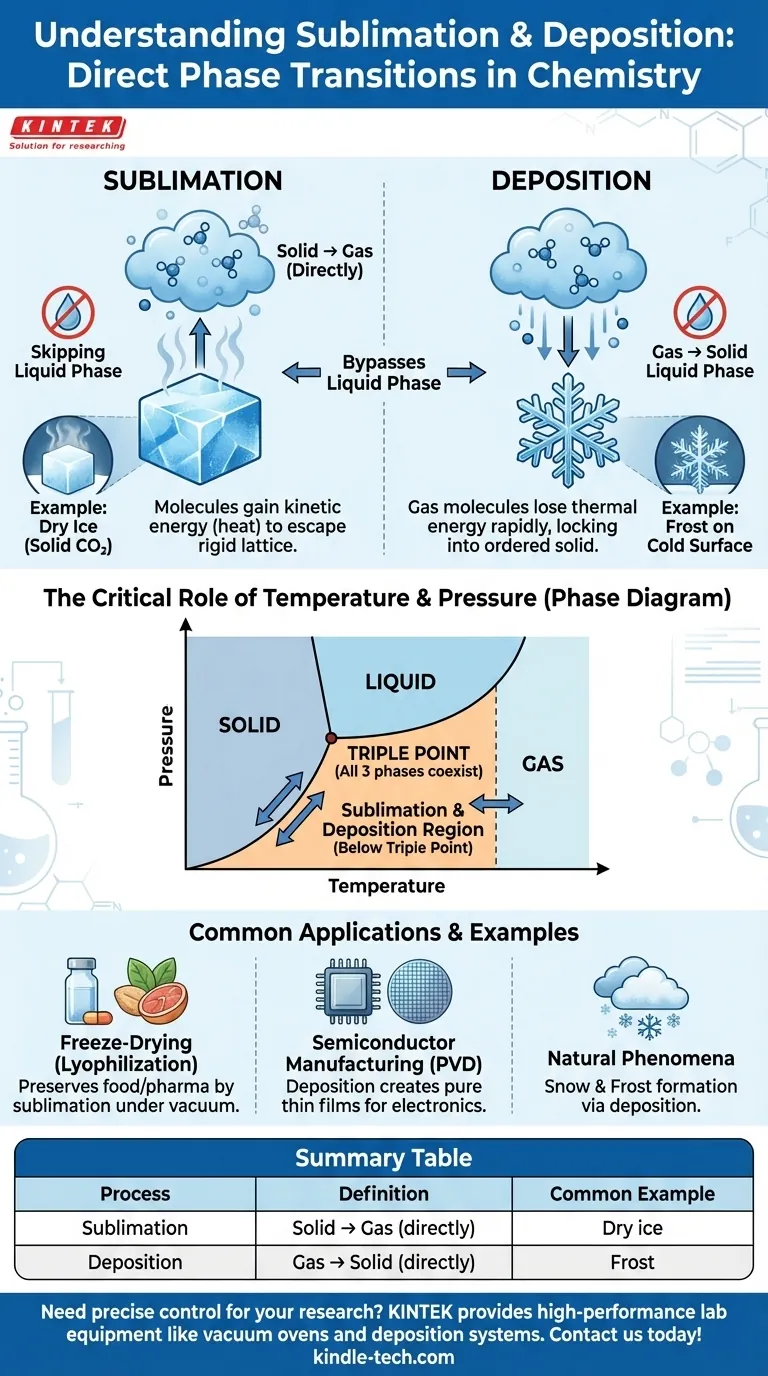
في دراسة المادة، التسامي والترسيب هما تحولا طور حيث تنتقل المادة مباشرة بين حالتيها الصلبة والغازية، متجاوزة الطور السائل تمامًا. التسامي هو التحول المباشر للمادة الصلبة إلى غاز. الترسيب هو العملية العكسية، حيث يتحول الغاز مباشرة إلى مادة صلبة.
المبدأ الأساسي الذي يجب فهمه هو أن التسامي والترسيب وجهان لعملة واحدة. إنهما يمثلان المسار المباشر ثنائي الاتجاه بين الطور الصلب والغازي الذي يحدث تحت ظروف محددة من درجة الحرارة والضغط، متجاوزًا الحالة السائلة الوسيطة بالكامل.

آلية تحولات الطور
لفهم سبب تخطي المادة للطور السائل، يجب أن ننظر إلى طاقة وترتيب جزيئاتها. تحولات الطور تتعلق أساسًا بالتغيرات في الطاقة الجزيئية وحرية الحركة.
التسامي: التحول من الصلب إلى الغاز
في المادة الصلبة، تكون الجزيئات مقفلة في بنية ثابتة، وغالبًا ما تكون بلورية، على الرغم من أنها لا تزال تهتز في مكانها.
عند إضافة الطاقة (عادةً في شكل حرارة)، تزداد هذه الاهتزازات. في التسامي، تكتسب الجزيئات طاقة حركية كافية للتغلب على القوى بين الجزيئية التي تبقيها في شبكتها الصلبة والهروب مباشرة كـ غاز.
مثال كلاسيكي هو الثلج الجاف، وهو ثاني أكسيد الكربون الصلب. في درجة حرارة الغرفة والضغط القياسي، يتحول مباشرة إلى ثاني أكسيد الكربون الغازي دون أن يصبح بركة سائلة أبدًا.
الترسيب: التحول من الغاز إلى الصلب
الترسيب هو عكس التسامي. يحدث عندما تفقد الجزيئات في الطور الغازي الطاقة الحرارية بسرعة.
هذا الفقدان السريع للطاقة يتسبب في تباطؤ جزيئات الغاز سريعة الحركة بشكل كبير لدرجة أنها تنغلق مباشرة في بنية صلبة منظمة. ليس لديها فرصة للتكثف في سائل أولاً.
تكوّن الصقيع على زجاج النافذة البارد هو مثال ممتاز. يتلامس بخار الماء الموجود في الهواء مع سطح أقل من درجة التجمد ويتحول مباشرة إلى بلورات ثلجية.
الدور الحاسم لدرجة الحرارة والضغط
ما إذا كانت المادة تتسامى أو تنصهر أو تغلي ليس خاصية متأصلة في المادة وحدها. يتم تحديده من خلال الظروف الخارجية لدرجة الحرارة والضغط، والتي يتم تصورها بشكل أفضل على مخطط الطور.
تقديم النقطة الثلاثية
لكل مادة، هناك تركيبة محددة من درجة الحرارة والضغط تسمى النقطة الثلاثية. هذه هي النقطة الفريدة التي يمكن أن تتعايش فيها الأطوار الصلبة والسائلة والغازية في توازن ديناميكي حراري.
لماذا يحدث تخطي الطور السائل
يحدث التسامي والترسيب عند مجموعات من درجات الحرارة والضغط أقل من النقطة الثلاثية.
عند هذه الضغوط المنخفضة، لا يكون الطور السائل مستقرًا. إضافة الطاقة إلى مادة صلبة ستدفعها مباشرة فوق الحد إلى الطور الغازي (التسامي)، وإزالة الطاقة من غاز ستجعله يعبر مباشرة إلى الطور الصلب (الترسيب).
التطبيقات والأمثلة الشائعة
هذه العمليات ليست مجرد مفاهيم نظرية؛ إنها محورية لكل من الظواهر الطبيعية والتقنيات الصناعية الحاسمة.
التسامي قيد التنفيذ: التجفيف بالتجميد
التجفيف بالتجميد (التجفيف بالتجميد) هو طريقة رئيسية لحفظ الأطعمة والمستحضرات الصيدلانية. يتم تجميد المادة أولاً، ثم يتم تقليل الضغط المحيط بشكل كبير، مما يتسبب في تسامي الماء المجمد (الثلج) مباشرة إلى بخار الماء، تاركًا العنصر جافًا دون تلف حراري.
الترسيب في التكنولوجيا: تصنيع أشباه الموصلات
في الصناعة التكنولوجية، تُستخدم عملية تسمى الترسيب الفيزيائي للبخار (PVD) لإنشاء أغشية رقيقة. يتم تبخير مادة صلبة في فراغ، ثم يترسب الغاز الناتج كغشاء صلب نقي على ركيزة، مثل رقاقة السيليكون المستخدمة في صنع رقائق الكمبيوتر.
الظواهر الطبيعية: الثلج والصقيع
تكوّن الثلج داخل السحب هو مثال طبيعي على الترسيب. يبرد بخار الماء في الغلاف الجوي ويترسب مباشرة إلى بلورات ثلجية معقدة، مكونًا رقاقات ثلجية لم تكن موجودة أبدًا كقطرات مطر سائلة.
اتخاذ الخيار الصحيح لهدفك
إن فهم هذه المفاهيم يسمح لك بتفسير كل من العمليات الطبيعية والصناعية بوضوح أكبر.
- إذا كان تركيزك الأساسي هو تصور الظواهر اليومية: تذكر أن "تدخين" الثلج الجاف هو تسامي، وأن الصقيع على العشب في صباح بارد هو ترسيب.
- إذا كان تركيزك الأساسي هو فهم العمليات الصناعية: أدرك أن التجفيف بالتجميد يستخدم التسامي لإزالة الماء بلطف، بينما يعتمد إنشاء الإلكترونيات المتقدمة غالبًا على الترسيب لبناء المكونات طبقة تلو الأخرى.
- إذا كان تركيزك الأساسي هو استيعاب الكيمياء الفيزيائية الأساسية: اربط فهمك بمخطط الطور، حيث يتضمن كل السلوك تحت النقطة الثلاثية انتقالات مباشرة من الصلب إلى الغاز.
في نهاية المطاف، يوضح التسامي والترسيب كيف أن حالة المادة هي حالة ديناميكية تحكمها التفاعلات بين الطاقة والضغط.
جدول ملخص:
| العملية | التعريف | مثال شائع |
|---|---|---|
| التسامي | صلب ← غاز (مباشرة) | الثلج الجاف (CO₂ صلب) يتحول إلى غاز |
| الترسيب | غاز ← صلب (مباشرة) | تكون الصقيع على نافذة باردة |
| الشرط الأساسي | يحدث عند درجات حرارة وضغوط أقل من النقطة الثلاثية للمادة | - |
هل تحتاج إلى تحكم دقيق في درجة الحرارة والضغط لأبحاث تحول الطور أو العمليات الصناعية الخاصة بك؟ تتخصص KINTEK في معدات المختبرات عالية الأداء، بما في ذلك أفران التفريغ وأنظمة الترسيب، لتحقيق الظروف اللازمة للتسامي والترسيب بشكل موثوق. دع خبرائنا يساعدونك في اختيار الأدوات المناسبة للتحديات الفريدة لمختبرك. اتصل بنا اليوم لمناقشة تطبيقك!
دليل مرئي