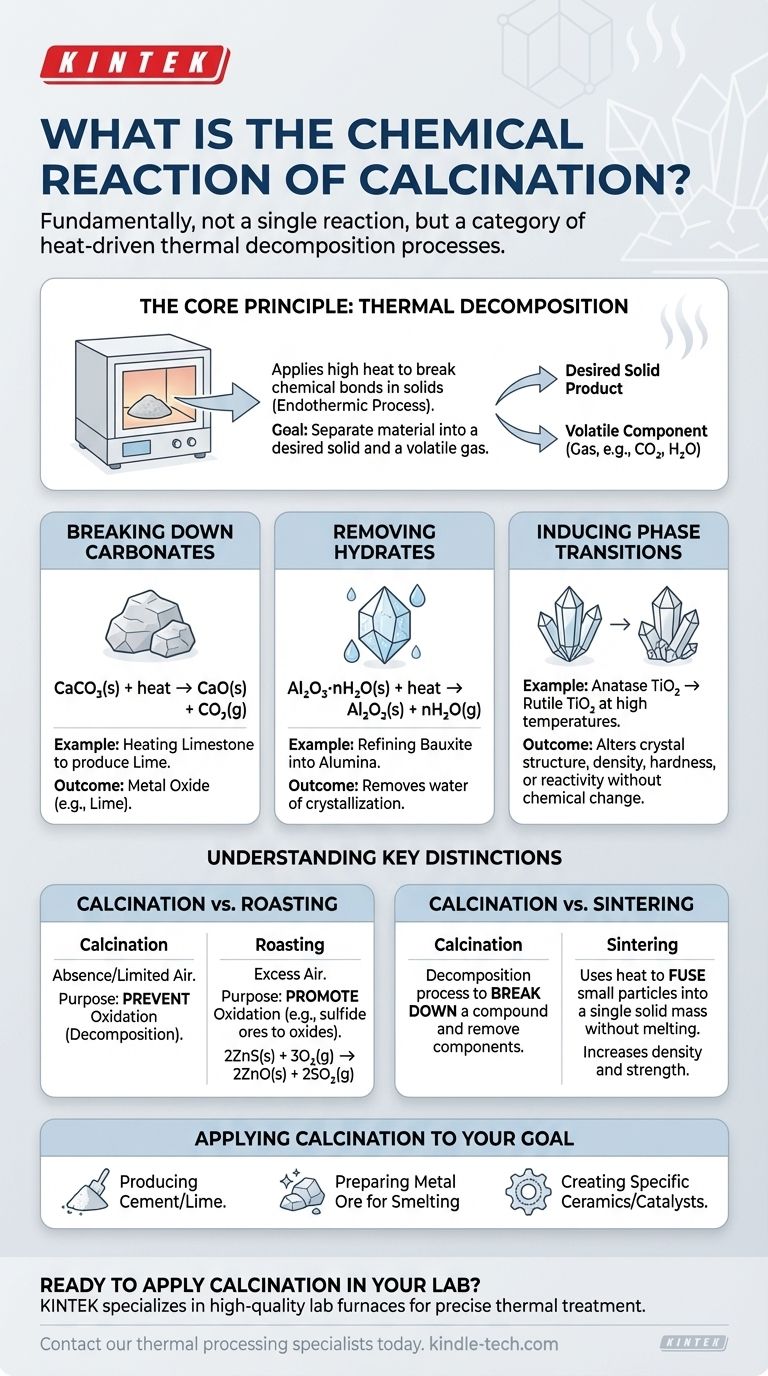
من الناحية الأساسية، التكليس ليس تفاعلاً كيميائياً واحداً بل هو فئة من العمليات المدفوعة بالحرارة والمحددة بنتيجة معينة: التحلل الحراري. في حين أن العديد من التفاعلات تندرج تحت هذا العنوان، فإن المثال الأكثر شيوعًا هو تفكك الكربونات، مثل تسخين الحجر الجيري (كربونات الكالسيوم) لإنتاج الجير (أكسيد الكالسيوم) وغاز ثاني أكسيد الكربون.
التكليس هو عملية معالجة حرارية تستخدم حرارة عالية في جو متحكم به لتفكيك المادة. الغرض الأساسي منه هو طرد المكون المتطاير - مثل ثاني أكسيد الكربون أو الماء - لتنقية أو تغيير الخصائص الكيميائية والفيزيائية للمادة الصلبة المتبقية.

المبدأ الأساسي: التحلل الحراري
يعمل التكليس عن طريق تطبيق طاقة حرارية كافية على مادة صلبة لكسر روابطها الكيميائية. هذه العملية ماصة للحرارة دائمًا، مما يعني أنها تتطلب مدخلات من الطاقة (الحرارة) للمضي قدمًا. الهدف هو فصل المادة إلى منتج صلب مرغوب فيه ومكون متطاير يمكن طرده كغاز.
تفكيك الكربونات
هذا هو التطبيق الكلاسيكي والأكثر انتشارًا للتكليس، خاصة في إنتاج الأسمنت. عندما يتم تسخين كربونات معدنية، فإنها تتحلل إلى أكسيد معدني وثاني أكسيد الكربون.
بالنسبة للحجر الجيري، يكون التفاعل:
CaCO₃(s) + heat → CaO(s) + CO₂(g)
هنا، تتحلل كربونات الكالسيوم الصلبة إلى أكسيد الكالسيوم الصلب (الجير) وثاني أكسيد الكربون الغازي.
إزالة الهيدرات (ماء التبلور)
توجد العديد من المعادن كـ "هيدرات"، مما يعني أن جزيئات الماء مدمجة في تركيبها البلوري. يستخدم التكليس لطرد هذا الماء، وهي عملية تسمى غالبًا "التجفيف"، على الرغم من أنها تحلل كيميائي.
على سبيل المثال، يتضمن تكرير خام البوكسيت إلى ألومينا تكليس أكسيد الألومنيوم المائي:
Al₂O₃·nH₂O(s) + heat → Al₂O₃(s) + nH₂O(g)
تزيل هذه الخطوة الماء، مما يركز أكسيد الألومنيوم، وهو مقدمة ضرورية لإنتاج الألومنيوم المعدني.
تحفيز التحولات الطورية
بشكل أقل شيوعًا، يمكن أن يشير التكليس إلى عملية لا يسبب فيها الحرارة تحللاً ولكنه يغير التركيب البلوري (الطور) للمادة. يؤدي هذا إلى تغيير خصائصها الفيزيائية، مثل الكثافة أو الصلابة أو التفاعلية، دون تغيير صيغتها الكيميائية.
أحد الأمثلة هو تحويل الأناتاز، وهو شكل من أشكال ثاني أكسيد التيتانيوم (TiO₂)، إلى طور الروتيل الأكثر استقرارًا في درجات الحرارة العالية.
فهم الفروق الرئيسية
تتضح قيمة التكليس عند مقارنتها بالعمليات الحرارية الشائعة الأخرى. تحدد الظروف المحددة - وخاصة الجو - النتيجة.
التكليس مقابل التحميص
هذا هو التمييز الأكثر أهمية. يحدث التكليس في غياب الهواء أو إمداد محدود به لمنع الأكسدة عن قصد.
في المقابل، يتم التحميص في وجود فائض من الهواء لتعزيز الأكسدة تحديدًا. يتم استخدامه عادةً على الخامات الكبريتيدية، وتحويلها إلى أكاسيد. على سبيل المثال، تحميص كبريتيد الزنك:
2ZnS(s) + 3O₂(g) → 2ZnO(s) + 2SO₂(g)
التكليس مقابل التلبيد
هذه العمليات لها أهداف متعاكسة. التكليس هو عملية تحلل تستخدم لتفكيك مركب وإزالة مكون منه.
أما التلبيد، فيستخدم الحرارة (أقل من درجة الانصهار) لصهر الجسيمات الصغيرة في كتلة صلبة واحدة. إنه يزيد الكثافة والقوة، ويقوم أساسًا بـ "لحام" المادة معًا دون صهرها.
تطبيق التكليس على هدفك
يعتمد تفاعل التكليس المحدد الذي تهتم به كليًا على المادة الأولية والمنتج النهائي المطلوب.
- إذا كان تركيزك الأساسي هو إنتاج الأسمنت أو الجير: فأنت تستخدم التكليس لتحليل كربونات الكالسيوم إلى أكسيد كالسيوم تفاعلي.
- إذا كان تركيزك الأساسي هو تحضير خام معدني للصهر: فمن المحتمل أنك تستخدم التكليس لإزالة الماء (من الهيدرات) أو ثاني أكسيد الكربون (من الكربونات) لإثراء المحتوى المعدني.
- إذا كان تركيزك الأساسي هو إنشاء سيراميك أو محفز محدد: فقد تكون تستخدم التكليس لتحقيق طور بلوري ومساحة سطح مرغوبة في مادة مثل الألومينا أو التيتانيا.
في نهاية المطاف، التكليس هو أداة أساسية في علم المواد لتحويل المواد الصلبة الخام إلى أشكال أكثر فائدة أو تركيزًا أو تفاعلية.
جدول الملخص:
| نوع تفاعل التكليس | مثال التفاعل | النتيجة الرئيسية |
|---|---|---|
| تحلل الكربونات | CaCO₃(s) + heat → CaO(s) + CO₂(g) |
ينتج أكسيد معدني (مثل الجير) |
| تحلل الهيدرات | Al₂O₃·nH₂O(s) + heat → Al₂O₃(s) + nH₂O(g) |
يزيل ماء التبلور |
| التحول الطوري | أناتاز TiO₂ → روتيل TiO₂ | يغير التركيب البلوري والخصائص |
هل أنت مستعد لتطبيق التكليس في مختبرك؟
سواء كنت تقوم بتطوير محفزات جديدة، أو معالجة خامات، أو تصنيع مواد سيراميكية متقدمة، فإن المعالجة الحرارية الدقيقة أمر بالغ الأهمية. تتخصص KINTEK في الأفران والمعدات المخبرية عالية الجودة المصممة لعمليات التكليس الموثوقة.
نحن نوفر الأدوات التي تحتاجها لتحقيق تسخين موحد، وتحكم دقيق في درجة الحرارة، ونتائج متسقة. دع خبرائنا يساعدونك في اختيار المعدات المناسبة لمادتك وتطبيقك المحدد.
اتصل بأخصائيي المعالجة الحرارية لدينا اليوم لمناقشة متطلبات مشروعك واكتشاف كيف يمكن لـ KINTEK تعزيز أبحاثك وتطويرك.
دليل مرئي
المنتجات ذات الصلة
- آلة مصنع فرن الانحلال الحراري بالفرن الدوار الكهربائي، فرن التكليس، فرن دوار صغير، فرن دوار
- فرن دوار كهربائي يعمل بشكل مستمر مصنع تحلل صغير فرن دوار تسخين
- فرن تفحيم الجرافيت الفراغي العمودي عالي الحرارة
- فرن تفحيم الجرافيت عالي الموصلية الحرارية
- فرن تفحيم الجرافيت الفراغي فائق الحرارة
يسأل الناس أيضًا
- ما هي مزايا فرن الفرن الدوار؟ تحقيق تجانس وكفاءة فائقة
- كيف يتم تسخين الأفران الدوارة؟ شرح طرق التسخين المباشر مقابل التسخين غير المباشر
- ما هي الصناعات التي تستخدم الأفران الدوارة؟ ضرورية للأسمنت والتعدين والمعالجة الكيميائية
- ما هي خصائص أنماط الحركة المنزلقة، والانهيار، والدحرجة للطبقة؟ تحسين عملية الدوران الخاصة بك
- ما هي مبادئ الفرن الدوار؟ إتقان ميكانيكا المعالجة في درجات الحرارة العالية



















