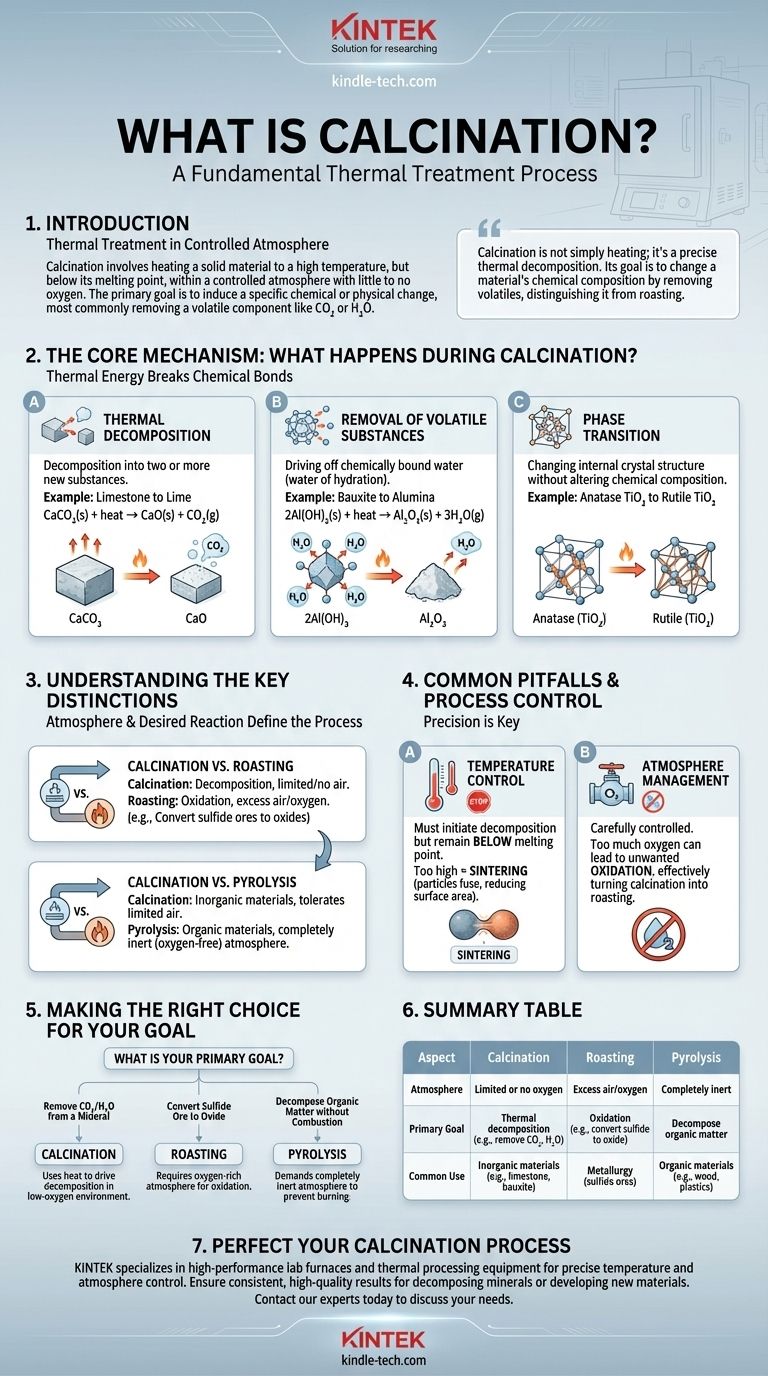
في علم المواد وعلوم الفلزات، يُعد التكليس عملية معالجة حرارية أساسية. وهي تنطوي على تسخين مادة صلبة إلى درجة حرارة عالية، ولكن أقل من نقطة انصهارها، وضمن جو مُتحكم فيه يحتوي على القليل أو لا يحتوي على أكسجين. لا تهدف هذه العملية إلى صهر المادة، بل إلى إحداث تغيير كيميائي أو فيزيائي محدد، وأكثرها شيوعًا هو إزالة مكون متطاير مثل ثاني أكسيد الكربون أو الماء.
التكليس ليس مجرد تسخين؛ إنه تحلل حراري دقيق. هدفه الأساسي هو تغيير التركيب الكيميائي للمادة عن طريق إزالة المكونات المتطايرة، مما يميزه عن المعالجات الحرارية الأخرى مثل التحميص، الذي ينطوي على تفاعل كيميائي مع جو الفرن.

الآلية الأساسية: ماذا يحدث أثناء التكليس؟
يعمل التكليس عن طريق توفير طاقة حرارية كافية لكسر الروابط الكيميائية، مما يؤدي إلى تحول متوقع للمادة الصلبة. يندرج هذا التغيير عادةً ضمن إحدى الفئات الثلاث.
التحلل الحراري
هذا هو الغرض الأكثر شيوعًا للتكليس. يتسبب الحرارة في تحلل المادة إلى مادتين جديدتين أو أكثر.
المثال النموذجي هو إنتاج الجير (أكسيد الكالسيوم) من الحجر الجيري (كربونات الكالسيوم). عند التسخين، تتحلل كربونات الكالسيوم، مطلقة غاز ثاني أكسيد الكربون وتاركة وراءها أكسيد الكالسيوم الصلب.
CaCO₃(s) + heat → CaO(s) + CO₂(g)
إزالة المواد المتطايرة
التكليس فعال للغاية في طرد الماء المرتبط كيميائيًا (ماء التبلور) من المعادن.
على سبيل المثال، في إنتاج الألومينا من البوكسيت، يُستخدم التكليس لتحويل هيدروكسيدات الألومنيوم إلى أكسيد الألومنيوم (الألومينا) عن طريق إزالة جزيئات الماء.
2Al(OH)₃(s) + heat → Al₂O₃(s) + 3H₂O(g)
التحول الطوري
بشكل أقل شيوعًا، يُستخدم التكليس لتغيير التركيب البلوري الداخلي للمادة (طورها) دون تغيير تركيبها الكيميائي.
تزيد هذه العملية من استقرار المادة أو تعدل خصائصها. على سبيل المثال، تسخين الأناتاز، وهو شكل من أشكال ثاني أكسيد التيتانيوم (TiO₂)، يحوله إلى طور الروتيل الأكثر استقرارًا وذا القيمة الصناعية.
فهم الفروق الرئيسية
غالبًا ما يتم الخلط بين مصطلح "التكليس" وعلاجات حرارية أخرى. يكمن الاختلاف الحاسم في الجو المستخدم و التفاعل الكيميائي المطلوب.
التكليس مقابل التحميص
النقطة الأكثر شيوعًا للالتباس هي بين التكليس و التحميص. في حين أن كلاهما يستخدم الحرارة، فإن أهدافهما وأجوائهما متعاكسة.
يتم التحميص في وجود فائض من الهواء أو الأكسجين. والغرض منه هو جعل المادة الصلبة تتفاعل مع الأكسجين، وعادةً ما يتم تحويل خامات الكبريتيد إلى أكاسيد.
على النقيض من ذلك، يتم التكليس في غياب الهواء أو في إمداد محدود جدًا به. والغرض منه هو التحلل، وليس الأكسدة.
التكليس مقابل الانحلال الحراري
الانحلال الحراري هو عملية تحلل حراري أخرى، ولكنه يُعرَّف باستخدامه لجو خامل تمامًا (خالٍ من الأكسجين).
يرتبط في الغالب بتحلل المواد العضوية، مثل إنتاج الفحم من الخشب. يُستخدم التكليس عادةً للمواد غير العضوية مثل المعادن ويمكنه تحمل كمية محدودة من الهواء، في حين أن الانحلال الحراري لا يمكنه ذلك.
المزالق الشائعة وضبط العملية
يتطلب التنفيذ الناجح للتكليس تحكمًا دقيقًا في المتغيرات الرئيسية. قد يؤدي الفشل في القيام بذلك إلى تفاعل غير مكتمل أو نواتج ثانوية غير مرغوب فيها.
التحكم في درجة الحرارة أمر بالغ الأهمية
يجب أن تكون درجة حرارة العملية عالية بما يكفي لبدء التحلل ولكنها تظل أقل من نقطة انصهار المادة.
إذا كانت درجة الحرارة مرتفعة جدًا، فقد يتسبب ذلك في التلبيد، حيث تبدأ الجزيئات في الاندماج. يقلل هذا من مساحة السطح وتفاعلية المنتج النهائي، وهو أمر غير مرغوب فيه غالبًا.
إدارة الجو
يتم التحكم بعناية في كمية الهواء أو الغاز المتفاعل في الفرن. يمكن أن يؤدي إدخال الكثير من الأكسجين إلى أكسدة غير مرغوب فيها، مما يحول عملية التكليس فعليًا إلى عملية تحميص.
اتخاذ الخيار الصحيح لهدفك
يعتمد اختيار المعالجة الحرارية الصحيحة بالكامل على المادة الأولية والمنتج النهائي الكيميائي المطلوب.
- إذا كان تركيزك الأساسي هو إزالة ثاني أكسيد الكربون أو الماء من معدن: التكليس هو العملية الصحيحة، لأنه يستخدم الحرارة لدفع التحلل في بيئة منخفضة الأكسجين.
- إذا كان تركيزك الأساسي هو تحويل خام الكبريتيد إلى أكسيد: التحميص هو العملية الضرورية، لأنه يتطلب جوًا غنيًا بالأكسجين لتسهيل تفاعل الأكسدة.
- إذا كان تركيزك الأساسي هو تحليل المادة العضوية دون احتراق: الانحلال الحراري هو الخيار الصحيح، لأنه يتطلب جوًا خاملًا تمامًا لمنع المادة من الاحتراق.
في نهاية المطاف، يتوقف اختيار المعالجة الحرارية الصحيحة على فهم ما إذا كنت تريد إزالة جزء من المادة أو مفاعلتها بشيء جديد.
جدول ملخص:
| الجانب | التكليس | التحميص | الانحلال الحراري |
|---|---|---|---|
| الجو | أكسجين محدود أو معدوم | هواء/أكسجين زائد | خامل تمامًا |
| الهدف الأساسي | التحلل الحراري (مثل إزالة ثاني أكسيد الكربون، H₂O) | الأكسدة (مثل تحويل الكبريتيد إلى أكسيد) | تحليل المواد العضوية |
| الاستخدام الشائع | المواد غير العضوية (مثل الحجر الجيري، البوكسيت) | علم الفلزات (خامات الكبريتيد) | المواد العضوية (مثل الخشب، البلاستيك) |
هل أنت مستعد لإتقان عملية التكليس الخاصة بك؟ تتخصص KINTEK في أفران المختبرات عالية الأداء ومعدات المعالجة الحرارية المصممة للتحكم الدقيق في درجة الحرارة والجو. سواء كنت تقوم بتحليل المعادن أو تطوير مواد جديدة، فإن حلولنا تضمن نتائج متسقة وعالية الجودة. اتصل بخبرائنا اليوم لمناقشة احتياجات مختبرك المحددة واكتشاف المعدات المناسبة لتطبيقك.
دليل مرئي
المنتجات ذات الصلة
- فرن دوار كهربائي يعمل بشكل مستمر مصنع تحلل صغير فرن دوار تسخين
- آلة مصنع فرن الانحلال الحراري بالفرن الدوار الكهربائي، فرن التكليس، فرن دوار صغير، فرن دوار
- فرن فرن عالي الحرارة للمختبر لإزالة الشوائب والتلبيد المسبق
- فرن صهر بالحث القوسي الفراغي
- فرن الضغط الساخن بالحث الفراغي 600 طن للمعالجة الحرارية والتلبيد
يسأل الناس أيضًا
- في أي درجة حرارة يحدث الانحلال الحراري؟ دليل للتحكم في إنتاج منتجك
- لماذا توجد سلاسل داخل فرن دوار؟ تعزيز الكفاءة والتحكم من خلال التبادل الحراري الداخلي
- ما هو فرن كهربائي دوار؟ حقق تسخينًا موحدًا فائقًا لموادك
- ما هي درجة حرارة الفرن الدوار؟ تعتمد على المواد وهدف العملية الخاصة بك
- ما هي الأنواع المختلفة لأفران الكلسنة؟ دليل لاختيار معدات المعالجة الحرارية المناسبة





